

���� ��1��A��һ�ֻ�ɫ���ʹ��壬��AΪS��BΪSO2��CΪSO3��
��2��A��һ�ֺ�ɫ���ʹ��壬AΪ̼��BΪCO��CΪCO2�����������������̼������Ӧ��2NaOH+CO2=Na2CO3+H2O��NaOH+CO2=NaHCO3���ݴ��ж�������Һ���������
��3��C�Ǻ���ɫ���壬CΪNO2����BΪNO��AΪN2��NH3��
��4��A��һ�ֻ��ý�����C�ǵ���ɫ���壬��AΪNa��BΪNa2O��CΪNa2O2����C����¶���ڿ����У���������DΪNa2CO3��
��� �⣺��1��A��һ�ֻ�ɫ���ʹ��壬��AΪS��BΪSO2��CΪSO3��B��C�Ļ�ѧ����ʽΪ��2SO2+O2$\frac{\underline{����}}{��}$2SO3��
�ʴ�Ϊ��2SO2+O2$\frac{\underline{����}}{��}$2SO3��
��2��A��һ�ֺ�ɫ���ʹ��壬AΪ̼��BΪCO��CΪCO2��̼��������ȼ�ϵȣ����������������̼������Ӧ��2NaOH+CO2=Na2CO3+H2O��NaOH+CO2=NaHCO3����������Һ���Լ��ԣ���ʱ��Һ����������ǵ�һ�ɷ֣�������Na2CO3��NaHCO3������Ƕ��ֳɷ֣������ǣ�Na2CO3��NaOH������Na2CO3��NaHCO3 ��
�ʴ�Ϊ��ȼ�ϣ�Na2CO3��NaHCO3��Na2CO3��NaOH��Na2CO3��NaHCO3 ��
��3��C�Ǻ���ɫ���壬CΪNO2����BΪNO��AΪN2��NH3��C��ˮ��Ӧ�����ӷ���ʽ��3NO2+H2O�T2H++2NO3-+NO����
�ʴ�Ϊ��N2��NH3��3NO2+H2O�T2H++2NO3-+NO����
��4��A��һ�ֻ��ý�����C�ǵ���ɫ���壬��AΪNa��BΪNa2O��CΪNa2O2������2Na2O2+2CO2=2Na2CO3+O2�����������ƿ�����������������C����¶���ڿ����У���������DΪNa2CO3��
����ʱ��������ٵ������Ƕ�����̼��ˮ����̼�����Ƶ�������xg��
2NaHCO3$\frac{\underline{\;\;��\;\;}}{\;}$Na2CO3+CO2��+H2O �����������
168g 62g
xg ��10-9.38��g=0.62g
168g��62g=xg��0.62g
���x=1.68gg��
��̼���Ƶ���������=$\frac{10g-1.68g}{10g}$��100%=83.2%��
�ʴ�Ϊ��2Na2O2+2CO2�T2Na2CO3+O2��Na2CO3��83.2%��
���� ���⿼��������ƶϣ���Ŀ�Ѷ��еȣ�ע��������ʵ���ɫ�����ƶϣ���������Ԫ�ػ��������ʣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ȼ����ڼ��Խ����и����ķ�Ӧʽ�ǣ�O2+2H2O+4e-=4OH- | |
| B�� | NaHCO3��ˮ��Һ�е�ˮ�����ӷ���ʽ��HCO3-+H2O?CO2��+OH- | |
| C�� | ��FeSΪ��������ȥ��ˮ�е�Hg2+��FeS��s��+Hg2+��aq��=HgS��s��+Fe2+ ��aq�� | |
| D�� | ���������绯ѧ��ʴ��������Ӧʽ��Fe-2e-=Fe2+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
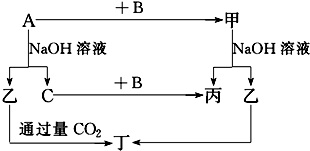
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
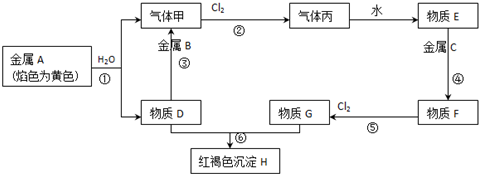
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
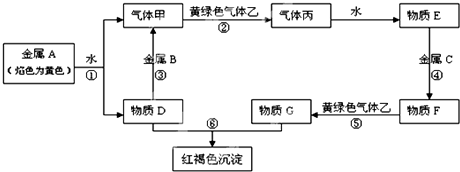
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �� ���� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0 |
| 1 | ||||||||
| 2 | A | |||||||
| 3 | B | C | D | E |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ͬ������N4��N5������ԭ����֮��Ϊ5��4 | |
| B�� | N5��N4��N2��Ϊͬ�������� | |
| C�� | N4��N5���������͵Ļ����� | |
| D�� | N5��Ħ������Ϊ70 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
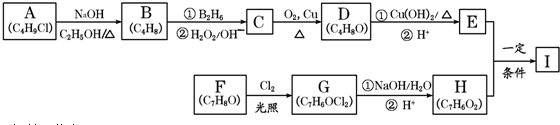
 ���÷�Ӧ����Ϊȡ����Ӧ��
���÷�Ӧ����Ϊȡ����Ӧ�� ��
�� ��
���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com