
| A. | 在饱和氯化铁溶液中滴加NaOH溶液,产生红褐色沉淀 | |
| B. | 水泥厂和冶金厂常用高压直流电除去大量烟尘,减少对空气的污染 | |
| C. | 清晨,在茂密的树林中,常常可以看到枝叶间透过的一道道光线 | |
| D. | 肾功能衰竭等疾病引起的血液中毒,可利用血液透析进行治疗 |
分析 胶体是分散质介于1-100nm的分散系,胶体具有丁达尔效应,能够发生电泳,产生据此,胶体能够透过滤纸但是不能够通过半透膜,以此解答该题.
解答 解:A.FeCl3溶液中逐滴加入NaOH溶液,发生复分解反应生成氢氧化铁沉淀,与胶体性质无关,故A选;
B.灰尘是胶体,在外加电源作用下,有电泳的性质,与胶体性质有关,故B不选;
C.清晨,在茂密的树林,常常可以看到从枝叶间透过的一道道光柱,属于胶体的丁达尔效应,故C不选;
D.血液中,蛋白质和血细胞颗粒较大,是胶体,不能透过透析膜,血液内的毒性物质直径较小,则可以透过,与胶体有关,故D不选;
故选A.
点评 本题考查胶体的性质,为高频考点,侧重于化学与生后的考查,有利于培养学生良好的科学素养,提高学生学习的积极性,明确胶体常见的性质有丁达尔现象、胶体的聚沉、电泳等以及利用胶体性质对生产生活中实际问题进行解释是解题关键,题目较简单.


 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案科目:高中化学 来源: 题型:解答题
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| H2O | CO | CO2 | CO | |||
| A | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
| B | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
| C | 1000 | 1 | 2 | c | d | t |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
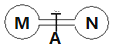 室温时,两个容积相同的烧瓶中分别盛有M和N两种气体(同温同压),取下弹簧夹A,使两烧瓶内的气体充分接触(如图),容器内的压强由大到小的顺序是( )
室温时,两个容积相同的烧瓶中分别盛有M和N两种气体(同温同压),取下弹簧夹A,使两烧瓶内的气体充分接触(如图),容器内的压强由大到小的顺序是( )| 编号 | ① | ② | ③ | ④ |
| 气体M | H2S | NH3 | HI | NO |
| 气体N | SO2 | HCl | Cl2 | O2 |
| A. | ③=④>①>② | B. | ③>④>①>② | C. | ④>③>②>① | D. | ④>③>①>② |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 根据反应MnO4-+5Fe2++8H+=Mn2-+5Fe3++4H2O可知,用酸性KMnO4溶液可检验FeSO4•7H2O是否变质 | |
| B. | 用CO2鉴别NaAlO2溶液和CH3COONa溶液 | |
| C. | 用湿润的碘化钾淀粉试剂鉴别Br2(g)和NO2 | |
| D. | 用KOH溶液鉴别SO3(g)和SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com