
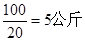 ,因此靠吃碘盐来预防放射性碘是不起作用的。
,因此靠吃碘盐来预防放射性碘是不起作用的。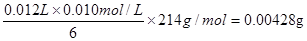 =4.28mg,加碘食盐中KIO3的含量为
=4.28mg,加碘食盐中KIO3的含量为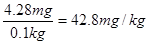 。其中含碘的质量是
。其中含碘的质量是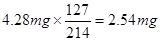
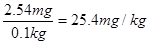 ,因此是合格产品。
,因此是合格产品。

科目:高中化学 来源:不详 题型:单选题
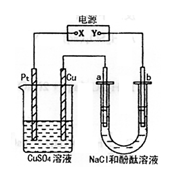
| A.x是正极,y是负极,CuSO4溶液的pH逐渐减小 |
| B.x是正极,y是负极,CuSO4溶液的pH保持不变 |
| C.烧杯中Pt电极上最多可析出铜0.64g |
| D.烧杯中Cu极上电极反应式4OH--4e-→2H2O+O2↑ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
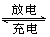 Fe(OH)2 +Ni(OH)2 下列推断中正确的是
Fe(OH)2 +Ni(OH)2 下列推断中正确的是| A.放电时,Fe是正极 |
| B.充电时阴极电极反应式为:Fe ( OH )2 + 2e-=Fe + 2OH- |
| C.充电时,Ni元素被还原 |
| D.放电时溶液中OH-移向正极 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
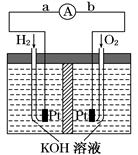
| A.氢气在负极发生氧化反应 |
| B.供电时的总反应为:2H2+O2=2H2O |
| C.产物为无污染的水,属于环境友好电池 |
| D.燃料电池的能量转化率可达100% |
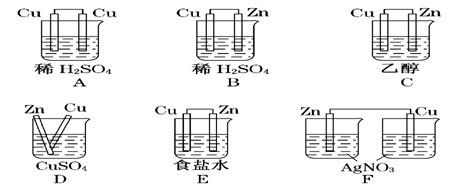
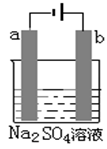
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题


| A.混合动力车上坡或加速时,溶液中的OH-向乙电极移动 |
| B.混合动力车刹车或下坡时,乙电极周围溶液的pH增大 |
| C.混合动力车上坡或加速时,乙电极电极反应式为 NiOOH+H2O+e-=Ni(OH)2+OH- |
| D.混合动力车刹车或下坡时,甲电极电极反应式为H2+2OH-+2e- =2H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.反应①、②中电子转移数目相等 | B.反应①中氧化剂是氧气和水 |
| C.三个反应都是氧化还原反应 | D.钢铁在潮湿的空气中不能发生电化学腐蚀 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.将铜铝导线焊接在一起使用 | B.将输送自来水的铁管表面镀锌 |
| C.经常用自来水冲洗生铁制品 | D.将输油铸铁管道埋在潮湿、疏松的土壤中 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

A.钢铁的腐蚀过程绝大多数都是电化学腐蚀 | B.在海轮外壳上镶入锌块,可减缓船体的腐蚀速率 | C.电解CuCl2饱和溶液,生成金属铜和氯气 | D.电解MgCl2饱和溶液,可制得金属镁 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.16g | B.32g | C.19.2g | D.12.8g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com