
短周期元素X原子核外的电子处于n个电子层上,最外层电子数为(2n+1),核内质子数为(2n2-1)。有关X的说法中不正确的是
| A.X元素气态氢化物的水溶液不可能呈酸性 |
| B.X能形成化学式为NaXO3的含氧酸钠盐 |
| C.X原子的最外层电子数和核电荷数不可能为偶数 |
| D.X元素常见单质的化学式为X2 |
科目:高中化学 来源: 题型:单选题
X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如右图所示。若Y原子的最外层电子数是次外层电子数的3倍,下列说法中正确的是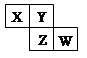
| A.原子半径:W>Z>Y>X |
| B.最高价氧化物对应水化物的酸性:Z>W>X |
| C.四种元素的单质中,Z单质的熔、沸点最低 |
| D.W的单质能与水反应,生成一种具有漂白性的物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
“嫦娥三号”,携带的“玉兔号”月球车使用的耐压外壳为钛合金。某种超高硬度钛合金的成分为Ti—6.5A1—6V一4Cr—0.5Si,该钛合金中硅元素在周期表中的位置为
| A.第三周期ⅣA族 | B.第三周期ⅢA族 |
| C.第四周期ⅣA族 | D.第四周期ⅣB族 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
长式周期表共有18个纵行,从左到右排为1~18列,即碱金属为第1列,稀有气体元素为第18列。按这种规定,下列说法正确的是
| A.第9列元素中有非金属元素 |
| B.只有第二列的元素原子最外层电子排布为ns2 |
| C.第四周期第8列元素是铁元素 |
| D.第15列元素原子的最外层电子排布为ns2np5 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知W、X、Y、Z为短周期元素,W、Z同主族,X、Y、Z同周期,W的气态氢化物的稳定性大于Z的气态氢化物的稳定性,X、Y为金属元素,X的阳离子的氧化性小于Y的阳离子的氧化性。下列说法正确的是( )
| A.X、Y、Z、W的原子半径依次减小 |
| B.W与X形成的化合物中只含离子键 |
| C.W的气态氢化物的沸点一定高于Z的气态氢化物的沸点 |
| D.若W与Y的原子序数相差5,则二者形成化合物的化学式一定为Y2W3 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知A、B、C、D、E是短周期元素,原子序数依次增大。其中A、E的单质在常温下呈气态, B的原子最外层电子数是其电子层数的2倍, C在同周期主族元素中原子半径最大, D的合金是日常生活中常用的金属材料。下列说法正确的是( )
A.B位于元素周期表中第二周期第ⅥA族
B.工业上可以用电解CE溶液的方法同时获得C、E单质
C.C、D的最高价氧化物对应的水化物之间能发生化学反应
D.化合物AE与CE具有相同类型的化学键
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
A、B、C、D是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中的两种或三种元素组成的化合物,辛是由C元素形成的单质。已知:甲+乙=丁+辛,甲+丙=戊+辛;常温下0.1 mol·L-1丁溶液的pH=13。下列说法中正确的是( )
A.元素B在周期表中的位置为第二周期第ⅥA族
B.元素B、C、D的原子半径由大到小的顺序为r(D)>r(C)>r(B)
C.1.0 L 0.1 mol·L-1戊溶液中阴离子总的物质的量小于0.1 mol
D.1 mol甲与足量的乙完全反应共转移了约6.02×1023个电子
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下图是部分短周期元素原子(用字母表示)最外层电子数与原子序数的关系图。下列说法正确的是(双选) ( )。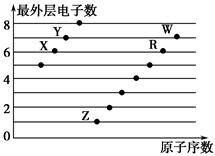
| A.X和R在同一周期 |
| B.原子半径:W>R>X |
| C.气态氢化物的稳定性:Y>X |
| D.X、Z形成的化合物中可能含有共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
元素的原子结构决定其性质和在周期表中的位置,下列说法中正确的是( )
A.元素周期表中位于金属和非金属分界线附近的元素属于过渡元素
B.某微粒的结构示意简图为 ,则该元素在周期表中位于第三周期、ⅥA族
,则该元素在周期表中位于第三周期、ⅥA族
C.过氧化氢电子式:
D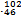 Pd和
Pd和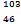 Pd互为同位素
Pd互为同位素
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com