
| A. | 用小苏打治疗胃酸过多:CO32-+2H+=CO2↑+H2O | |
| B. | 稀硝酸中加入过量的铁粉:Fe+4H++NO3-=Fe2++NO↑+2H2O | |
| C. | Ba(HCO3)2溶液中加入过量的NaOH溶液:2HCO3-+Ba2++2OH-=BaCO3↓+2H2O+CO32- | |
| D. | 用惰性电极电解饱和氯化镁溶液:2Cl-+2H2O $\frac{\underline{\;通电\;}}{\;}$2OH-+H2↑+Cl2↑ |
分析 A.小苏打为碳酸氢钠,离子方程式中碳酸氢根离子不能拆开;
B.离子方程式两边正电荷不相等;
C.氢氧化钠过量,反应生成碳酸钡沉淀、碳酸钠和水;
D.氢氧根离子与镁离子结合生成氢氧化镁沉淀.
解答 解:A.用小苏打治疗胃酸过多,碳酸氢根离子不能拆开,正确的离子方程式为:HCO3-+H+=CO2↑+H2O,故A错误;
B.稀硝酸中加入过量的铁粉,反应生成硝酸亚铁、NO气体和水,正确的离子方程式为:3Fe+8H++NO3-=3Fe2++2NO↑+4H2O,故B错误;
C.Ba(HCO3)2溶液中加入过量的NaOH溶液,反应的离子方程式为:2HCO3-+Ba2++2OH-=BaCO3↓+2H2O+CO32-,故C正确;
D.用惰性电极电解氯化镁溶液,反应生成氢气、氯气和氢氧化镁沉淀,正确的离子反应为:Mg2++2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$Mg(OH)2↓+H2↑+Cl2↑,故D错误;
故选C.
点评 本题考查了离子方程式的书写判断,为高考的高频题,属于中等难度的试题,注意明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)等.


 名题金卷系列答案
名题金卷系列答案科目:高中化学 来源: 题型:选择题
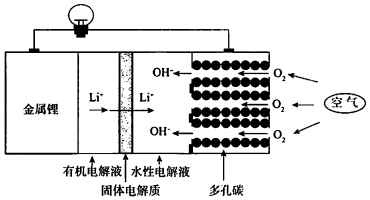
| A. | 回收水性电解液可制取锂 | |
| B. | 可将有机电解液改为水溶液 | |
| C. | 正极的电极反应式为O2+4e-+2H2O═4OH- | |
| D. | 电池总反应方程式为4Li+O2+2H2O═4LiOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(A)=2.0mol•L-1•min-1 | B. | v(B)=4.0mol•L-1•min-1 | ||
| C. | v(C)=0.1mol•L-1•s-1 | D. | v(D)=0.3mol•L-1•s-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ①③ | C. | ②④ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
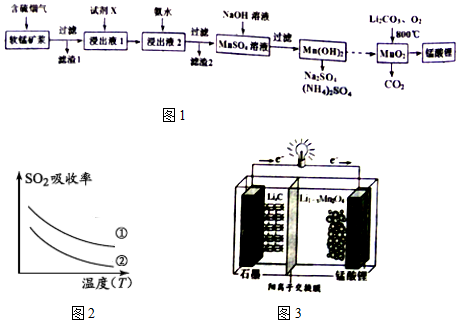
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 3.4 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 4.7 | 9.8 |
| 实验序号 | SO2浓度(g•m-3) | 烟气流速(mL•min-1) |
| ① | 4.1 | 55 |
| ② | 4.1 | 96 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol 庚烷分子中含共价键 23 NA | |
| B. | 所有烷烃分子中均存在极性键和非极性键 | |
| C. | C2H4、C2H4Br2、CH2Cl2均只能代表一种物质 | |
| D. | A、B 两种烃,它们含碳质量分数相同,则 A 和 B 最简式一定相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | CuO作还原剂 | B. | 铜元素化合价降低 | ||
| C. | CuO作氧化剂 | D. | 铜元素被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 投入足量漂白粉后的溶液中:Fe2+、H+、Cl-、SO42- | |
| B. | 0.1mol/LFeCl3溶液中:Na+、Ba2+、NO3-、SCN- | |
| C. | $\frac{{K}_{w}}{c({H}^{+})}$=1×10-13mol/L的溶液中:NH4+、Ca2+、Cl、NO3- | |
| D. | 水电离的c(OH-)=1×10-13mol/L的溶液中:K+、Na+、AlO2-、CO32- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com