
”¾ĢāÄæ”æĻĀĮŠÓŠ¹ŲĶ¼ĻńµÄĖµ·ØÕżČ·µÄŹĒ
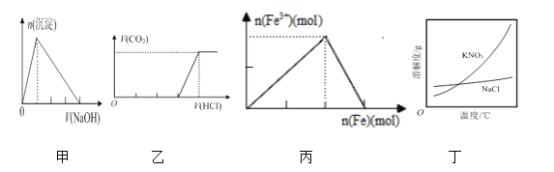
A. Ķ¼¼×±ķŹ¾£ŗĻņijĆ÷·ÆČÜŅŗÖŠµĪ¼Ó¹żĮæµÄNaOHČÜŅŗ£¬Éś³É³ĮµķµÄĪļÖŹµÄĮæÓėµĪ¼ÓNaOHČÜŅŗĢå»żµÄ¹ŲĻµ
B. Ķ¼ŅŅ±ķŹ¾£ŗĻņŗ¬µČĪļÖŹµÄĮæµÄNaOHŗĶNa2CO3µÄ»ģŗĻČÜŅŗÖŠµĪ¼Ó¹żĮæµÄĻ”ŃĪĖį£¬Éś³ÉĘųĢåµÄĢå»żÓėµĪ¼ÓHClČÜŅŗĢå»żµÄ¹ŲĻµ
C. Ķ¼±ū±ķŹ¾£ŗŌŚĻ”ĻõĖįČÜŅŗÖŠ¼ÓČė¹żĮæµÄĢś·Ū£¬ČÜŅŗÖŠFe3+ĪļÖŹµÄĮæÓė¼ÓČėĢś·ŪĪļÖŹµÄĮæµÄ±ä»Æ¹ŲĻµ
D. øł¾ŻĶ¼¶”£¬³żČ„»ģŌŚKNO3ÖŠÉŁĮæµÄNaClæÉÓĆ”°Õō·¢ÅØĖõ”¢³ĆČČ¹żĀĖ”±µÄ·½·Ø
”¾“š°ø”æC
”¾½āĪö”æ
A. ĻņijĆ÷·ÆČÜŅŗÖŠµĪ¼ÓNaOHČÜŅŗÖ±ÖĮ¹żĮ棬ČÜŅŗÖŠĻČÉś³É³Įµķ£¬Č»ŗó³ĮµķÓÖÖš½„Čܽā£¬Ē°ŗóĮ½øö½×¶ĪƻӊĻūŗĵÄĒāŃõ»ÆÄĘČÜŅŗµÄĢå»żÖ®±ČĪŖ3:1£¬Ķ¼ĻńÓėÖ®²»·ū£¬A“ķĪó£»
B. ¼ŁÉčNaOHŗĶNa2CO3·Ö±šĪŖ1mol£¬Ļņŗ¬ÓŠ1molNaOHŗĶNa2CO3µÄ»ģŗĻČÜŅŗÖŠµĪ¼Ó¹żĮæµÄĻ”ŃĪĖį£¬ĒāŃõ»ÆÄĘĻČÓėŃĪĖį·“Ó¦ĻūŗÄ1molHCl£»Ģ¼ĖįÄĘÓėŃĪĖį·“Ӧɜ³É1molNaHCO3£¬ĻūŗÄHCl 1mol£»×īŗó1molNaHCO3ŌŁÓėŃĪĖį·“Ó¦²śÉś¶žŃõ»ÆĢ¼ĘųĢ壬ÓÖĻūŗÄHCl 1mol£¬ĖłŅŌ²śÉśĘųĢåĒ°ŗóĻūŗÄŃĪĖįµÄĢå»żÖ®±ČĪŖ2:1£¬Ķ¼ĻńÓėÖ®²»·ū£¬B“ķĪó£»
C. ŌŚĻ”ĻõĖįČÜŅŗÖŠ¼ÓČėĢś·Ū£¬ĻČ·¢ÉśFe+2NO3-+4H+=Fe3++2NO”ü+2H2O£¬µ±ĻõĖįĻūŗÄĶźÖ®ŗó£¬ĢśĄė×ÓµÄĮæ“ļµ½×ī“óÖµ£»¼ĢŠų¼ÓČėĢś·Ūŗó£¬ĢśĄė×ÓÓėĢś·¢Éś·“Ó¦£¬Fe+2Fe3£«£½3Fe2£«£¬ĢśĄė×ÓµÄĮæÖš½„¼õŠ”Ö±ÖĮĪŖ0£¬×īÖÕĮ½²½·“Ó¦ĻūŗÄĢśµÄĮæĪŖ1:0.5=2:1£¬ÓėĶ¼ĻńĻą·ūŗĻ£¬CÕżČ·£»
D. KNO3Čܽā¶ČĖęĪĀ¶Č±ä»Æ½Ļ“ó£¬ĀČ»ÆÄĘČܽā¶ČĖęĪĀ¶Č±ä»Æ²»“ó£¬Ņņ“Ė³żČ„»ģŌŚKNO3ÖŠÉŁĮæµÄNaClæÉÓĆ”°Õō·¢ÅØĖõ”¢ĄäČ“½į¾§”¢¹żĀĖ”±µÄ·½·Ø½ųŠŠ·ÖĄė£¬D“ķĪó£»
×ŪÉĻĖłŹö£¬±¾ĢāŃ”C”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖCeO2Ķس£¼Č²»ČÜÓŚĒæĖį£¬Ņ²²»ČÜÓŚĒæ¼ī”£Ä³¹¤³§ŅŌĘ½°åµēŹÓĻŌŹ¾ĘĮ³§µÄ·Ļ²£Į§·ŪÄ©£Øŗ¬CeO2”¢SiO2”¢Fe2O3”¢FeOµČĪļÖŹ£©ĪŖŌĮĻ£¬Éč¼ĘČēĻĀĶ¼ĖłŹ¾¹¤ŅÕĮ÷³Ģ£¬ÖĘµĆ“æ¾»µÄCeO2”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©

A. ŹµŃéŹŅÖŠ£¬²Ł×÷3ŗĶ²Ł×÷1”¢²Ł×÷2ĖłÓĆŅĒĘ÷²»Ķ¬
B. ĀĖŌüÖŠ¼ÓČėĻ”H2SO4ŗĶH2O2£¬ĘäÖŠH2O2×öŃõ»Æ¼Į
C. ĀĖŅŗÖŠCe3+ÓėNaOH”¢O2µÄ·“Ó¦ŹōÓŚ»ÆŗĻ·“Ó¦
D. ²Ł×÷2·ÖĄėµĆµ½µÄĀĖŌüÖŠŅ»¶Øŗ¬ÓŠĪ“·“Ó¦µÄSiO2
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŃŠ¾æČĖŌ±ŃŠÖĘ³öŅ»ÖÖæÉ×÷ĪŖÓćĄ×ŗĶĒ±Ķ§µÄ“¢±øµēŌ“µÄŠĀŠĶµē³Ų”Ŗ”Ŗļ®Ė®µē³Ų(½į¹¹ČēĶ¼)£¬Ź¹ÓĆŹ±¼ÓČėĖ®¼“æɷŵē”£ĻĀĮŠ¹ŲÓŚøƵē³ŲµÄĖµ·Ø²»ÕżČ·µÄŹĒ(””””)
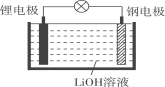
A. ļ®ĪŖøŗ¼«£¬øÖĪŖÕż¼«B. ¹¤×÷Ź±øŗ¼«µÄµē¼«·“Ó¦Ź½ĪŖLi£e££½Li£«
C. ¹¤×÷Ź±OH£ĻņøÖµē¼«ŅʶÆD. ·ÅµēŹ±µē×ÓµÄĮ÷Ļņ£ŗļ®µē¼«”śµ¼Ļß”śøÖµē¼«
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĪŖ³«µ¼”°½ŚÄܼõÅÅ”±ŗĶ”°µĶĢ¼¾¼Ć”±£¬ÄæĒ°¹¤ŅµÉĻÓŠŅ»ÖÖ·½·ØŹĒÓĆCO2Ą“Éś²śČ¼ĮĻŅŅ“¼”£Ņ»¶ØĢõ¼žĻĀ·¢Éś·“Ó¦£ŗ2CO2(g)£«6H2(g)![]() CH3CH2OH(g)£«3H2O(g)””¦¤H<0”£
CH3CH2OH(g)£«3H2O(g)””¦¤H<0”£
£Ø1£©ŌŚŅ»¶ØĢõ¼žĻĀ£¬ŌŚ20 LĆܱÕČŻĘ÷ÖŠ°“ĪļÖŹµÄĮæ±ČĪŖ1”Ć3³äČėCO2ŗĶH2£¬ĪĀ¶ČŌŚ450 K£¬n(H2)Ėꏱ¼ä±ä»ÆČē±ķĖłŹ¾£ŗ
t/min | 0 | 1 | 3 | 5 |
n(H2)/mol | 8 | 6 | 5 | 5 |
ŌŚ450 ”ę”¢0”«1 min£¬v(CH3CH2OH)£½________£»“ĖĪĀ¶ČĻĀøĆ·“Ó¦µÄ»ÆŃ§Ę½ŗā³£ŹżĪŖ________(½į¹ū±£ĮōČżĪ»ÓŠŠ§Źż×Ö)”£
£Ø2£©ŌŚ5 MPaĻĀ²āµĆĘ½ŗāĢåĻµÖŠø÷ĪļÖŹµÄĢå»ż·ÖŹżĖęĪĀ¶ČµÄ±ä»ÆĒśĻßČēĶ¼ĖłŹ¾£ŗ

ĒśĻßŅŅ±ķŹ¾µÄŹĒ ________(ĢīĪļÖŹµÄ»ÆѧŹ½)µÄĢå»ż·ÖŹż£¬Ķ¼ĻńÖŠAµć¶ŌÓ¦µÄĢå»ż·ÖŹżb£½________%(½į¹ū±£ĮōČżĪ»ÓŠŠ§Źż×Ö)”£
£Ø3£©ĻĀĮŠ“ėŹ©ÖŠÄÜŹ¹»ÆŃ§Ę½ŗāĻņÕż·“Ó¦·½ĻņŅĘ¶ÆµÄŹĒ________”£
A£®ÉżøßĪĀ¶Č
B£®½«CH3CH2OH(g)¼°Ź±Ņŗ»Æ³é³ö
C£®Ń”Ōńøߊ§“߻ƼĮ
D£®ŌŁ³äČėl mol CO2ŗĶ3 mol H2
£Ø4£©25 ”ę”¢1.01”Į105PaŹ±£¬9.2 gŅŗĢ¬ŅŅ“¼ĶźČ«Č¼ÉÕ£¬µ±»Öø“µ½ŌדĢ¬Ź±£¬·Å³ö273.4 kJµÄČČĮ棬Š“³ö±ķŹ¾ŅŅ“¼Č¼ÉÕµÄČČ»Æѧ·½³ĢŹ½£ŗ________________________”£
£Ø5£©ŅŌŹÆÄ«ĪŖµē¼«£¬ĒāŃõ»ÆÄĘ”¢ŅŅ“¼”¢Ė®”¢ŃõĘųĪŖŌĮĻ£¬æÉŅŌÖĘ³ÉŅŅ“¼µÄČ¼ĮĻµē³Ų£¬Š“³ö·¢Éś»¹Ō·“Ó¦µÄµē¼«·“Ó¦Ź½£ŗ_____________________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¶ĢÖÜĘŚM”¢NĮ½ÖÖŌŖĖŲ¶ŌÓ¦µÄ¼ņµ„Ąė×Ó·Ö±šĪŖmMa+”¢n Nb-£¬ČōĄė×ÓµÄŗĖĶāµē×ÓÅŲ¼ĻąĶ¬£¬ŌņĻĀĮŠ¹ŲĻµ²»ÕżČ·µÄŹĒ£Ø £©
A. Ō×Ó°ė¾¶£ŗM < NB. Ąė×Ó°ė¾¶£ŗM < N
C. Ō×ÓŠņŹż£ŗM > ND. Ö÷×åŠņŹż£ŗM < N
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÖŲøõĖį¼ŲŹĒŅ»ÖÖÖŲŅŖµÄ»Æ¹¤ŌĮĻ£¬¹¤ŅµÉĻÓÉøõĢśæó£ØÖ÷ŅŖ³É·ÖĪŖFeOCr2O3”¢SiO2µČ£©Öʱø£¬ÖʱøĮ÷³ĢČēĶ¼ĖłŹ¾£ŗ
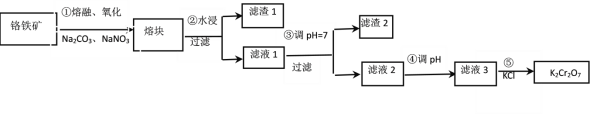
ŅŃÖŖ£ŗa.²½Öč¢ŁµÄÖ÷ŅŖ·“Ó¦ĪŖ£ŗ2FeOCr2O3+4Na2CO3+ 7NaNO3 ![]() 4Na2CrO4+Fe2O3+4CO2+7NaNO2£¬b. 2CrO42-+2H+
4Na2CrO4+Fe2O3+4CO2+7NaNO2£¬b. 2CrO42-+2H+ ![]() Cr2O72-+H2O£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
Cr2O72-+H2O£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A. ²½Öč¢ŁČŪČŚ”¢Ńõ»ÆæÉŅŌŌŚĢÕ“ÉČŻĘ÷ÖŠ½ųŠŠ
B. ²½Öč¢ŁÖŠĆæÉś³É44.8L CO2¹²×ŖŅĘ7molµē×Ó
C. ²½Öč¢ÜČōµ÷½ŚĀĖŅŗ2µÄpHŹ¹Ö®±äŠ”£¬ŌņÓŠĄūÓŚÉś³ÉCr2O72”Ŗ
D. ²½Öč¢ŻÉś³ÉK2Cr2O7¾§Ģ壬ĖµĆ÷øĆĪĀ¶ČĻĀK2Cr2O7Čܽā¶ČŠ”ÓŚNa2Cr2O7
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ”°ĀĢÉ«»Æѧ”±ŹĒµ±½ńÉē»įĢį³öµÄŅ»øöŠĀøÅÄī”£ŌŚ”°ĀĢÉ«»Æѧ”±¹¤ŅÕÖŠ£¬ĄķĻėדĢ¬ŹĒ·“Ó¦ĪļÖŠµÄŌ×ÓČ«²æ×Ŗ»ÆĪŖÓūÖĘµÄ²śĪļ£¬¼“Ō×ÓĄūÓĆĀŹĪŖ100%”£ĻĀĮŠ·“Ó¦×ī·ūŗĻĀĢÉ«»Æѧ֊”°Ō×Ó¾¼Ć”±ŅŖĒóµÄŹĒ
A. nCH2=CH2![]()
![]()
B. CH4£«2Cl2![]() CH2Cl2£«2HCl
CH2Cl2£«2HCl
C. Cl2£«2NaOH===NaCl£«NaClO£«H2O
D. 3NO2£«H2O===2HNO3£«NO
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”潫Ņ»¶ØĮæ“æ¾»µÄ°±»ł¼×Ėįļ§£ØNH2COONH4£©ÖĆÓŚĢŲÖʵÄĆܱÕÕęæÕČŻĘ÷ÖŠ(¼ŁÉčČŻĘ÷Ģå»ż²»±ä£¬¹ĢĢåŹŌŃłĢå»żŗöĀŌ²»¼Ę)£¬ŌŚŗć¶ØĪĀ¶ČĻĀŹ¹Ęä“ļµ½·Ö½āĘ½ŗā£ŗNH2COONH4£Øs£©![]() 2NH3£Øg£©+CO2£Øg£©,ĻĀĮŠæÉŅŌÅŠ¶ĻøĆ·Ö½ā·“Ó¦ŅŃ¾“ļµ½»ÆŃ§Ę½ŗāדĢ¬µÄŹĒ( )
2NH3£Øg£©+CO2£Øg£©,ĻĀĮŠæÉŅŌÅŠ¶ĻøĆ·Ö½ā·“Ó¦ŅŃ¾“ļµ½»ÆŃ§Ę½ŗāדĢ¬µÄŹĒ( )
A. 2v£ØNH3£©=v(CO2) B. ĆܱÕČŻĘ÷ÖŠ×ÜŃ¹Ēæ²»±ä
C. ĆܱÕČŻĘ÷ÖŠ»ģŗĻĘųĢåµÄĘ½¾łÄ¦¶ūÖŹĮæ²»±ä D. ĆܱÕČŻĘ÷ÖŠ°±ĘųµÄĢå»ż·ÖŹż²»±ä
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æH2ŗĶI2ŌŚŅ»¶ØĢõ¼žĻĀÄÜ·¢Éś·“Ó¦£ŗH2(g) + I2(g)![]() 2HI(g) ¦¤H£½£a kJ”¤mol£1
2HI(g) ¦¤H£½£a kJ”¤mol£1
ŅŃÖŖ£ŗ (a”¢b”¢c¾ł“óÓŚĮć)
(a”¢b”¢c¾ł“óÓŚĮć)
ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ( )
A. ·“Ó¦ĪļµÄ×ÜÄÜĮæøßÓŚÉś³ÉĪļµÄ×ÜÄÜĮæ
B. ¶ĻæŖ1 mol H£H¼üŗĶ1 mol I£I¼üĖłŠčÄÜĮæ“óÓŚ¶ĻæŖ2 mol H£I¼üĖłŠčÄÜĮæ
C. ¶ĻæŖ2 mol H£I¼üĖłŠčÄÜĮæŌ¼ĪŖ(c+b+a) kJ
D. ĻņĆܱÕČŻĘ÷ÖŠ¼ÓČė2 mol H2ŗĶ2 mol I2£¬³ä·Ö·“Ó¦ŗó·Å³öµÄČČĮæŠ”ÓŚ2a kJ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com