
(1)NaOH溶液:_______________________________________________________
(2)稀HNO![]() :_______________________________________________________
:_______________________________________________________
(3)澄清石灰水:_______________________________________________________
科目:高中化学 来源: 题型:
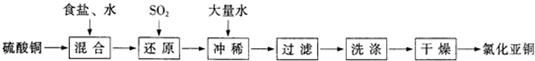
| H2O |
查看答案和解析>>
科目:高中化学 来源:三明一模 题型:填空题
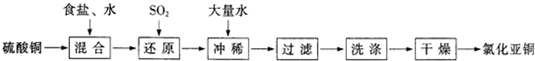
| H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
下图所示为常见气体制备、分离、干燥和性质验证的部分仪器装置(加热设备及夹持固定装置均略去),请根据要求完成下列各题(仪器装置可任意选用,必要时可重复选择,a、b为活塞)。
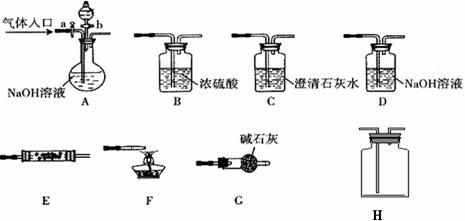
(1)实验前,如何检查A装置的气密: 。
(2)若气体入口通入CO和CO2的混合气体,E内放置CuO,选择装置获得纯净干燥的CO,并验证其还原性及氧化产物,所选装置的连接顺序为 (填代号)。能验证CO氧化产物的现象是 。
(3)若A中气体入口改通空气,分液漏斗内改加浓氨水,圆底烧瓶内改加NaOH固体,E内放置铂铑合金网,H为空瓶,D中改为石蕊试液,按A→G→E→H→D装置顺序制取干燥的氨气,并验证氨的某些性质。
①装置A中能产生氨气的原因有 。
②实验中先用酒精灯加热催化管,再通入混合气体,可观察到H内有红棕色气体出现,D中石蕊试液变红,则E中发生反应的方程式为 。
③若把酒精灯撤去,继续通入气体,催化剂可继续保持红热状态,反应继续进行。能使催化剂继续保持红热的原因是: 。
④某同学在做上述实验时出现了与其他同学不同的现象,他发现催化剂红热现象明显而正常,但石蕊试液不变红。请分析可能的原因:(答两点即可)
。
查看答案和解析>>
科目:高中化学 来源:2009年福建省三明市高考化学一模试卷(解析版) 题型:填空题
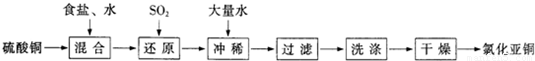
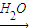 CuCl↓+Cl-.
CuCl↓+Cl-.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com