
| A. | ① | B. | ② | C. | ③ | D. | ②③ |
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:选择题
| A. | K+、Mg2+、CO32-、Cl- | B. | Na+、Ba2+、HCO3-、OH- | ||
| C. | Mg2+、H+、Cl-、SO42- | D. | K+、SO42-、Cu2+、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
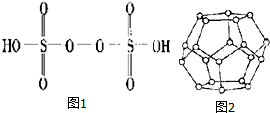
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 糖类、油脂、蛋白质在一定条件下均可以水解 | |
| B. | SiO2既能溶于NaOH溶液又能溶于HF,说明SiO2是两性氧化物 | |
| C. | 从海水中得到氯化镁晶体,电解氯化镁晶体可获得金属Mg | |
| D. | 锅炉水垢中含有的CaSO4,可先用Na2CO3溶液处理,后用酸除去 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷与氯气在光照的条件下反应,乙烯制氯乙烷 | |
| B. | 乙烷在氧气中燃烧,甲苯使酸性高锰酸钾溶液褪色 | |
| C. | 乙烯水化法制乙醇,乙醇浓硫酸170℃制乙烯 | |
| D. | 乙块制氯乙烯,苯的溴代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H4Cl2有三种同分异构体 | |
| B. | 将苯与浓硝酸和浓硫酸共热制取硝基苯 | |
| C. | 将红热的铜丝迅速插入无水乙醇中可将乙醇氧化为乙醛 | |
| D. | 可用浓硝酸鉴别淀粉溶液和鸡蛋白溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | x+y<z | B. | 平衡逆向移动 | C. | A的转化率降低 | D. | C的体积分数升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2种 | B. | 4种 | C. | 6种 | D. | 8种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com