
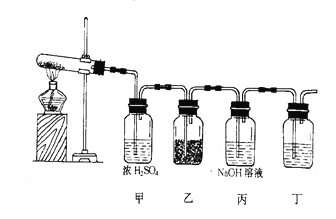
【题目】在下图装置中,加热试管内的白色固体A(A的焰色反应为黄色),生成白色固体B并放出气体C和D,这些气体通过甲瓶的浓硫酸后,C被吸收;D进入乙瓶跟另一淡黄色固体E反应生成白色固体B和气体F;丙瓶中的NaOH溶液用来吸收剩余的气体D。
(1)写出各物质的化学式:
A______; B_______; C________; D______; E_______; F___________。
(2)写出试管中及丙瓶中反应的化学方程式:_______________;__________________。
(3)等物质的量A、B分别与足量的盐酸反应生成气体的体积________(填“一样多”、“前者多”、“后者多”)。
【答案】 NaHCO3 Na2CO3 H2O CO2 Na2O2 O2 2NaHCO3![]() Na2CO3+H2O+CO2↑ CO2+2NaOH==Na2CO3+H2O 一样多
Na2CO3+H2O+CO2↑ CO2+2NaOH==Na2CO3+H2O 一样多
【解析】加热白色固体A(A灼烧时火焰为黄色)生成白色固体B,并放出气体C和D,则A、B含有Na元素,气体D与淡黄色固体E反应,生成固体B和气体F,应是Na2O2与CO2反应生成Na2CO3与O2,可推知D为CO2,E为Na2O2,B为Na2CO3,F为O2,故A为NaHCO3,C为水蒸气。
(1)根据以上分析可知A是NaHCO3,B是Na2CO3,C是H2O,D是CO2,E是Na2O2,F是O2。(2)根据以上分析可知试管中及丙瓶中反应的化学方程式分别为2NaHCO3![]() Na2CO3+H2O+CO2↑、CO2+2NaOH==Na2CO3+H2O。(3)等物质的量A、B中碳原子的物质的量相等,则分别与足量的盐酸反应生成气体的体积一样多。
Na2CO3+H2O+CO2↑、CO2+2NaOH==Na2CO3+H2O。(3)等物质的量A、B中碳原子的物质的量相等,则分别与足量的盐酸反应生成气体的体积一样多。


 计算高手系列答案
计算高手系列答案科目:高中化学 来源: 题型:
【题目】含氮化合物的研发与绿色反展、经济可持续发展有着密切关联.
(1)氨是一种重要化工原料.合成氨原料气H2 , 可用天然气为原料制得,有关反应能量变化如图1所示.则用CH4(g)和H20(g)反应制得H2(g)和CO(g)的热化学方程式为:
(2)氮的氧化物有着广泛用途,又是环境的污染物.(i)在150℃时,将0.4mol NO2气体充入体积为2L的真空密闭容器中,发生反应:2NO2(g)N2O4(g).
每隔一定时间测定容器内各物质的物质的量,数据如下表:
时间/S | 0 | 20 | 40 | 60 | 80 |
N(NO2)/mol | 0.4 | n1 | 0.26 | n3 | n4 |
N(N2O4)/mol | 0 | 0.05 | n2 | 0.08 | 0.08 |
①当反应在150℃达到平衡时,该反应平衡常数K= . (填数值)
②若最初通入N2O4 , 在相同条件下达到平衡时,各物质浓度仍然相同,则N2O4的起始浓度
应为 .
(ii)氨氧化制HNO3的尾气中含有NO和NO2 , 且n(NO):n(NO2)=1:1,可用尿素溶液除去,其作用原理是:NO2和NO与水反应生成亚硝酸,亚硝酸再与尿素[CO( NH2)2]反应生成对环境无污
染的物质.若用1mol尿素吸收该尾气,则能吸收氮氧化物g.
(3)氨气,CO2在一定条件下可合成尿素,其反应为:2NH3(g)+CO2(g)═CO(NH2)2(s)+H2O(g)图2表示合成塔中氨碳比a与CO2转化率ω的关系.a为[n(NH3):n(CO2)],b为水碳比[n(H2O):n(CO2)].则:
①b应控制在;
A.1.5~1.6 B.1~1.1 C.0.6~0.7
②a应控制在4.0的理由是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 6.02×1023个分子的体积约是22.4 L
B. 0.5 mol H2的体积为11.2 L
C. 1 mol气体的体积为22.4 L,则一定是在标准状况下
D. 标准状况下,体积相同的气体所含的分子数相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取Xg镁和铝的混合物,向其中加入适量的稀盐酸,恰好完全反应生成标准状况下的气体BL向反应后的溶液中加入VmLCmol/L氢氧化钠溶液,使金属离子刚好沉淀完全,得到的沉淀质量为Yg.再将得到的沉淀灼烧至质量不再改变为止,得到固体Pg.则下列关系不正确的是( )
A.![]() X<P<
X<P< ![]() X
X
B.P=X+ ![]()
C.Y=X+V?C
D.C= ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F是六种短周期主族元素,它们的原子序数依次增大,其中A、D及C、F分别是同一主族元素,A、F两元素的原子核中质子数之和比C、D两元素原子核中质子数之和少2,F元素的最外层电子数是次外层电子数的0.75倍.又知B元素的最外层电子数是内层电子数的2倍,E元素的最外层电子数等于其电子层数.请回答:
(1)1mol由E、F二种元素组成的化合物跟由A、C、D三种元素组成的化合物发生反应,完全反应后消耗后者的物质的量为 .
(2)A、C、F间可形成甲、乙两种微粒,它们均为负一价双原子阴离子,甲有18个电子,乙有10个电子,则甲与乙反应的离子方程式为 .
(3)单质B的燃烧热a kJ/mol.由B、C二种元素组成的化合物BC 14 g完全燃烧放出b kJ热量,写出单质B和单质C反应生成BC的热化学方程式: .
(4)工业上在高温的条件下,可以用A2C和BC反应制取单质A2 . 在等体积的Ⅰ、Ⅱ两个密闭容器中分别充入1molA2C和1mol BC、2mol A2C和2mol BC.一定条件下,充分反应后分别达到平衡(两容器温度相等).下列说法正确的是
A.达到平衡所需要的时间:Ⅰ>Ⅱ
B.达到平衡后A2C的转化率:Ⅰ=Ⅱ
C.达到平衡后BC的物质的量:Ⅰ>Ⅱ
D.达到平衡后A2的体积分数:Ⅰ<Ⅱ
E.达到平衡后吸收或放出的热量:Ⅰ=Ⅱ
F.达到平衡后体系的平均相对分子质量:Ⅰ<Ⅱ
(5)用B元素的单质与E元素的单质可以制成电极浸入由A、C、D三种元素组成的化合物的溶液中构成电池,则电池负极的电极反应式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D是中学化学的常见物质,它们在一定条件下有如下转化关系:A ![]() B
B ![]() C
C
(1)若A为能使湿润的红色石蕊试纸变蓝的气体,C为红棕色气体.则A的空间构型为 , A转化为B反应的化学方程式为 .
(2)若A、B、C均为氧化物,A为砖红色固体,且A中金属元素为+1价,D是一种黑色固态非金属单质,则A的化学式为 , B的电子式为 .
(3)若D为氯碱工业的主要产品,B为高中常见的一种具有两性的物质,则C溶液中除氢氧根外还存在的阴离子的化学式为 . 氯碱工业中阴极的电极反应式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在图所示物质的转化关系中,D在常温下为无色无味的液体(反应条件均已省略).请回答下列问题:
(1)高温下发生的反应②中,若F为常见的金属单质,H是非金属单质,用化学方程式表示G的一个重要用途: .
(2)若F为淡黄色粉末,①写出反应②的化学方程式并用双线桥标出电子转移的方向和数目 .
②F的电子式 .
(3)若A是一种强酸,B是一含有两种金属元素的盐,且其水溶液显碱性,写出①反应的离子方程式 .
(4)若A、F、H是短周期且相邻的两个族的元素单质,且反应均在溶液中进行,请写出:①的离子方程式;
②的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下有①4.48L CH4;②6.02×1023个HCl;③13.6g H2S;④0.3molNH3。下列对四种气体的关系从小到大表示不正确的是
A. 体积 ①<④<③<② B. 密度 ①<④<③<②
C. 质量 ①<④<③<② D. 氢原子数①<④<③<②
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com