
| A、滴定前对碱式滴定管仰视读数,滴定后又俯视 |
| B、滴定前锥形瓶内含有少量水 |
| C、滴定前,碱式滴定管尖嘴部分有气泡,滴定后气泡消失 |
| D、碱式滴定管用蒸馏水洗净后,直接装入已知浓度的NaOH溶液 |
| c(标准)×V(标准) |
| V(待测) |
| c(标准)×V(标准) |
| V(待测) |
| c(标准)×V(标准) |
| V(待测) |
| c(标准)×V(标准) |
| V(待测) |
| c(标准)×V(标准) |
| V(待测) |


 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:
| A、78gNa2O2固体中含有的阴离子数为NA(相对原子质量 Na:23 O:16 H:1) |
| B、标准状况下,11.2L乙烯含有的共价键数目为3 NA |
| C、在0℃,101千帕时,金属钠从水中置换出22.4LH2,发生转移的电子数为2NA |
| D、在25℃,pH=13的NaOH溶液中含有的OH-数约为6.02×1022 |
查看答案和解析>>
科目:高中化学 来源: 题型:
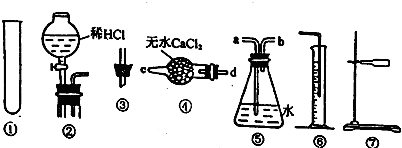
 某校化学兴趣小组对一款锌铁合金中铁的含量进行测定,该小组提出用测定产生氢气的体积的方法来进行实验.实验过程中需要读取氢气体积.
某校化学兴趣小组对一款锌铁合金中铁的含量进行测定,该小组提出用测定产生氢气的体积的方法来进行实验.实验过程中需要读取氢气体积.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 6
6
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:



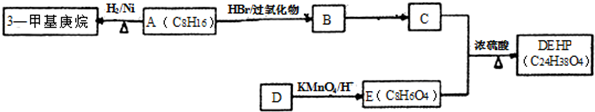
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com