
(12分)甲醇是一种很好的燃料,工业上可用多种原料通过不同的反应制得甲醇。
(1)已知在常温常压下:
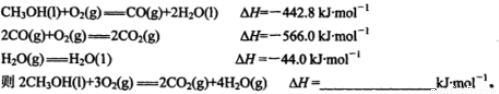
(2)工业上正在研究利用CO2和H2来生产甲醇燃料的方法,该反应为:
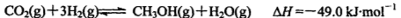
在某温度下,将6mol CO2和8mol H2 充入容积为2L的密闭容器中,8分钟时达平衡状态,H2的转化率为75%。请回答:
①用CH3OH表示该反应在0-8min内的平均反应速率v(CH3OH) = .
②此温度下该反应平衡常数K=____________;
③若在上述平衡体系中,再充入2mol H2,反应达到平衡后H2的转化率_________75% (填“大于”、“小于”或“等于”)。
(3) 一氧化碳与氢气也可以合成甲醇: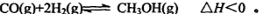
①若该反应在恒温恒容条件下进行,下列说法正确的是 ;
a.若混合气体的密度不再改变,说明反应已达化学平衡状态
b.反应达到平衡后,通入CH3OH(g)使压强增大,平衡向右移动
c.反应达到平衡后,通入氩气使压强增大,平衡向右移动
d.反应达到平衡后,升高温度,平衡逆向移动,平衡常数减小
e.若使用催化剂,会改变反应的途径,但反应的焓变不变
②某温度下,在一个容积为2L的密闭容器中进行该反应,已知此温度下的平衡常数
K=50 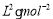 ,反应到某时刻测得各组分的物质的量如下:
,反应到某时刻测得各组分的物质的量如下:

请比较此时正、逆反应速率的大小:v正 v逆(填“>”、“<”或“=”)
(12分,每空2分)
(1)-1275.6 KJ·min-1
(2)① 0.125 mol·L-1·min-1 ②0.5 L2·mol-2 ③小于
(3)① d e ② =
【解析】
试题分析:(1)根据盖世定律可知,要求反应的?H=2?H1+?H2—4?H3,带入各反应的数据可得?H=-1275.6 KJ·min-1
(2)①根据“三段式 ”进行计算,CO2+ 3H2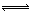 CH3OH+H2O
CH3OH+H2O
起始浓度(mol?L?1) 3 4 0 0
转化浓度(mol?L?1) 1 3 1 1
平衡浓度(mol?L?1) 2 1 1 1
v(CH3OH) =1mol/L÷8min=0.125 mol·L-1·min-1。
②平衡常数K=1mol/L×1mol/L÷[2mol/L×(1mol?L?1)3]= 0.5 L2·mol-2
③若在上述平衡体系中,再充入2mol H2,H2起始浓度增大,所以反应达到平衡后H2的转化率减小,小于75%。
(3)①a、反应热器为恒温恒容,气体体积为定值,根据质量守恒定律,气体的质量为定值,所以混合气体的密度为定值,则混合气体的密度不再改变,不能说明反应已达化学平衡状态,错误;b、反应达到平衡后,通入CH3OH(g),生成物的浓度增大,平衡向左移动,错误;c、反应达到平衡后,通入氩气,反应体系中各物质浓度不变,平衡不移动,错误;d、该反应为放热反应,所以反应达到平衡后,升高温度,平衡逆向移动,平衡常数减小,正确;e、若使用催化剂,会改变反应的途径,根据盖斯定律,反应的焓变不变,正确。
②根据表中数据可求出浓度商,Q=0.4mol/L÷[0.2mol?L?1×(0.2mol?L?1)2]= 50 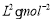 = K,说明此时反应处于平衡状态,则v正=v逆。
= K,说明此时反应处于平衡状态,则v正=v逆。
考点:本题考查盖斯定律、化学平衡状态的判断、化学平衡移动及相关计算。


 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案科目:高中化学 来源:2015届山东省济宁市高三10月阶段测试化学试卷(解析版) 题型:选择题
下列除去杂质的方法正确的是( )
A.除去N2中的少量O2:通过灼热的CuO粉末,收集气体
B.除去FeCl2溶液中的少量FeCl3:加入足量铁屑,充分反应后,过滤
C.除去CO2中的少量HCl:通入Na2CO3溶液,收集气体
D.除去KCl溶液中的少量MgCl2:加入适量NaOH溶液,过滤
查看答案和解析>>
科目:高中化学 来源:2015届山东省高三上学期第一次(10月)检测化学试卷(解析版) 题型:选择题
能正确表示下列反应的离子方程式是 ( )
A.浓盐酸与铁屑反应:2Fe+6H+===2Fe3++3H2↑
B.钠与CuSO4溶液反应:2Na+Cu2+===Cu↓+2Na+
C.NaHCO3溶液与稀H2SO4反应:CO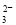 +2H+===H2O+CO2↑
+2H+===H2O+CO2↑
D.向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2+2Fe3+===2Fe(OH)3↓+3Mg2+
查看答案和解析>>
科目:高中化学 来源:2015届山东省高三上学期第二次检测化学试试卷(解析版) 题型:选择题
FeCl3、CuCl2的混合溶液中加入铁粉,充分反应后仍有固体存在,则下列判断不正确是
A.加入KSCN溶液一定不变红色
B.溶液中一定含Cu2+
C.溶液中一定含Fe2+
D.剩余固体中一定含铜
查看答案和解析>>
科目:高中化学 来源:2015届山东省高三上学期第二次检测化学试试卷(解析版) 题型:选择题
下列实验中所选用的仪器或实验基本操作合理的是
①用50 mL量筒量取5.2 mL稀硫酸; ②用酒精洗涤粘有硫粉的试管;
③用托盘天平称量10.1 g氯化钠晶体; ④用饱和NaHCO3溶液除之CO2中的少量SO2;
⑤用瓷坩埚熔融NaOH固体; ⑥实验中不慎将手指划破,可立即用FeCl3溶液止血
A.①②③④ B.③④⑥
C.③④⑤ D.③⑤⑥
查看答案和解析>>
科目:高中化学 来源:2015届山东省高三第一次学情调查化学试卷(解析版) 题型:选择题
在密闭容器中充入一定量的NO2,发生反应2NO2(g) 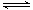 N2O4(g) ΔH=-57 kJ·mol-1。在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如图所示。下列说法正确的是( )
N2O4(g) ΔH=-57 kJ·mol-1。在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如图所示。下列说法正确的是( )

A.a、c两点的反应速率:a>c
B.a、b两点NO2的转化率:a<b
C.a、c两点气体的颜色:a深,c浅
D.由a点到b点,可以用加热的方法
查看答案和解析>>
科目:高中化学 来源:2015届山东省高三第一次学情调查化学试卷(解析版) 题型:选择题
处于平衡状态的反应2H2S(g)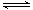 2H2(g)+S2(g) ΔH>0,不改变其他条件的情况下合理的说法是
2H2(g)+S2(g) ΔH>0,不改变其他条件的情况下合理的说法是
A.加入催化剂,反应路径将发生改变,ΔH也将随之改变
B.升高温度,正逆反应速率都增大,H2S分解率也增大
C.增大压强,平衡向逆反应方向移动,将引起体系温度降低
D.若体系恒容,注入一些H2后达新平衡,H2浓度将减小
查看答案和解析>>
科目:高中化学 来源:2015届山东省文登市高三上学期11月月考化学试卷(B卷)(解析版) 题型:选择题
下列由相关实验现象所推出的结论正确的是
A.铁在常温下不溶于浓硝酸,说明铁与浓硝酸不反应
B.将氯气溶于水后溶液呈浅黄绿色,说明氯气与水没有完全反应
C.将某气体通入品红溶液中溶液褪色,说明该气体一定是二氧化硫
D.向溶液中滴加盐酸酸化的BaCl2溶液出现白色沉淀,说明该溶液中一定有SO42-
查看答案和解析>>
科目:高中化学 来源:2015届山东省德州市高三10月月考化学试卷(解析版) 题型:选择题
对于4℃时100mL水中溶解了22.4 L HCl气体(标准状况下测得)后形成的溶液,下列说法中正确的是
A.该溶液物质的量浓度为10moL/L
B.所得的溶液的体积为22.5L
C.根据题干数据,该溶液物质的量浓度无法求得
D.该溶液中溶质的质量分数因溶液的密度未知而无法求得
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com