
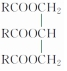 ”来表示,其中R为碳原子数目多于10的链烃基,可以相同也可以不同.分子式为C51H92O6的某油脂在稀硫酸中加热水解后得到A、B两种物质,若A的相对分子质量为92(已知:R1-CH═CH-R2$→_{H+}^{KMnO_{4}}$R1-COOH+R2-COOH),则
”来表示,其中R为碳原子数目多于10的链烃基,可以相同也可以不同.分子式为C51H92O6的某油脂在稀硫酸中加热水解后得到A、B两种物质,若A的相对分子质量为92(已知:R1-CH═CH-R2$→_{H+}^{KMnO_{4}}$R1-COOH+R2-COOH),则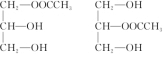 .
. 分析 分子式为C51H92O6的某油脂在稀硫酸中加热水解,涉及反应为C51H92O6+3H2O→A+B,A的相对分子质量为92,应为CH2OHCHOHCH2OH,由质量守恒可知B的分子式为C16H30O2,方程式为C51H92O6+3H2O→CH2OHCHOHCH2OH+3C16H30O2,B$→_{H+}^{KMnO_{4}}$C+D,等物质的量的C、D分别与足量的NaOH溶液反应时,消耗的NaOH的质量之比为1:2,C、D的相对分子质量相差30且C、D结构中均无支链,可知D为二元酸,应含有2个羧基,C含有1个羧基,可知C为CH3(CH2)6COOH,D为HOOC(CH2)6COOH,以此解答该题.
解答 解:(1)由以上分析可知B为C16H30O2,A为CH2OHCHOHCH2OH,
故答案为:C16H30O2;CH2OHCHOHCH2OH;
(2)质量守恒可知B的分子式为C16H30O2,B$→_{H+}^{KMnO_{4}}$C+D,等物质的量的C、D分别与足量的NaOH溶液反应时,消耗的NaOH的质量之比为1:2,C、D的相对分子质量相差30且C、D结构中均无支链,可知D为二元酸,应含有2个羧基,C含有1个羧基,可知C为CH3(CH2)6COOH,D为HOOC(CH2)6COOH,
则B的结构简式为CH3(CH2)6CH═CH(CH2)6COOH,
故答案为:CH3(CH2)6CH═CH(CH2)6COOH;
(3)A为CH2OHCHOHCH2OH,相对分子质量为92,与乙酸在一定条件下反应后生成相对分子质量为134的E,而乙酸的相对分子质量为60,则可知1molA与1mol乙酸发生酯化反应,可能生成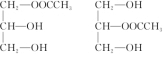 ,故答案为:
,故答案为: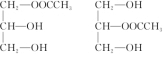 .
.
点评 本题考查有机推断,为高考常见题型和高频考点,题目难度较大,试题涉及的知识点较多、综合性较强、计算量较大,熟练掌握常见有机物结构与性质为解答关键,注意把握好确定有机物分子式、结构简式的方法,试题充分考查了学生的分析、理解能力及化学计算能力.


 全优点练单元计划系列答案
全优点练单元计划系列答案科目:高中化学 来源: 题型:选择题
| A. | 1molNa2O2固体中含离子总数为4 NA | |
| B. | 分子数为NA的CO、C2H4混合气体体积约为22.4L,质量为28g | |
| C. | 28g由C2H4和C3H6组成的混合物中含有氢原子的数目为4NA | |
| D. | 常温下,1mol Fe与过量浓HNO3反应,转移电子的数目为3 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 若用AG来表示溶液的酸度,其表达式为:AG=lg[$\frac{c({H}^{+})}{c(O{H}^{-})}$].298K时,用0.1mol/L的盐酸溶液滴定10mL 0.1mol/L 的MOH溶液,滴定曲线如图所示:下列说法正确的是( )
若用AG来表示溶液的酸度,其表达式为:AG=lg[$\frac{c({H}^{+})}{c(O{H}^{-})}$].298K时,用0.1mol/L的盐酸溶液滴定10mL 0.1mol/L 的MOH溶液,滴定曲线如图所示:下列说法正确的是( )| A. | 该滴定实验最好选择酚酞作为指示剂 | |
| B. | C点时加入盐酸溶液的体积等于10 mL | |
| C. | 滴定过程中从A点到D点,溶液中水的电离程度先逐渐减小,后逐渐增大 | |
| D. | 若B点加入的盐酸溶液体积为5mL,则所得溶液中:c(M+)+2c(H+)═c(MOH)+2c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
| 4 | ⑩ |
 .
. 或
或
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com