
【题目】反应A+3B==2C+4D(A、B、C、D均为气态),在四种不同情况下的反应速率最快的是
A. v(A)=0.1mol/(L·s) B. v(B) =0.6mol/(L·s)
C. v(C) =0.6mol/(L·s) D. v(D) =0.8mol/(L·s)
科目:高中化学 来源: 题型:
【题目】研究小组发现一种化合物在一定波长的光照射下发生分解反应,反应物浓度随反应时间变化如图所示。则反应10min时反应物的浓度和反应4min-8min间的平均反应速率,结果应是
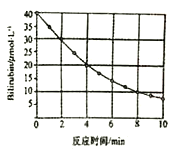
A. 7.5mol/L和2.5mol/(L·min) B. 7.5μmol/L和2.5umol/(L·min)
C. 0.75umol/L和3.0u(L·min) D. 0.75mol/L和5.0umol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应2A(g) + B(g) ![]() C(g) + 3D(g),达到平衡时,下列说法正确的是( )
C(g) + 3D(g),达到平衡时,下列说法正确的是( )
A. A、B全部变成了C和D
B. A、B、C、D四种物质的浓度一定相等
C. 反应速率为零
D. 单位时间内B消耗的物质的量和B生成的物质的量相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NO2是大气的主要污染物之一,某研究小组设计如图所示的装置对NO2进行回收利用,装置中a、b均为多孔石墨电极。下列说法不正确的是
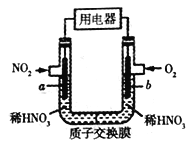
A. a为电池的负极,发生氧化反应
B. 一段时间后,b极附近HNO3 浓度减小
C. 电池总反应为4NO2+O2+2H2O![]() 4HNO3
4HNO3
D. 电子流向:a电极→用电器→b电极→溶液→a电极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用相同浓度的NaOH 溶液,分别滴定等体积且浓度均为0.1mol/L的三种酸(HA、HB 和HD)溶液,滴定的曲线如图所示,下列判断正确的是

A. 三种酸的电离常数关系:K(HD)>K(HB)>K(HA)
B. pH=7 时,三种溶液中:c(A-)=c(B-)=c(D-)
C. 当三种酸中和百分数达100%时,离子总浓度最大的是NaD 溶液
D. 滴定至P点时,溶液中:c(B-)>c(Na+)>c(HB)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外兴趣小组用右图装置进行实验,试回答: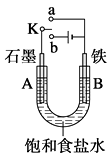
(1)若开始时开关K与a连接,则A电极反应式为。
(2)若开始时开关K与b连接,这种方法经常用于金属的防护,这种防护措施叫做 , 则A电极反应式为;B电极反应式为。
(3)开关K与b连接,将饱和食盐水换成CuSO4溶液,则A电极反应式为 , 该反应的离子方程式为 ,电解一段时间后(溶液仍然为蓝色),溶液的pH值将(填“变大”、“变小”、“不变”),若将电解质溶液恢复至原状,应补充 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以氧化铝为原料,通过碳热还原法可合成氮化铝(AlN);通过电解法可制取铝。电解铝时阳极产生的CO2可通过二氧化碳甲烷化等再利用。请回答:
(1)已知:①.2Al2O3(s)=4Al(g)+3O2(g) △H1=+3351kJ/mol
②. 2C(s)+ O2(g)=2CO(g) △H2=-221kJ/mol
③. 2Al(g)+ N2(g)=2AlN(s) △H3=a kJ/mol
④. Al2O3(s)+ 3C(s)+ N2(g)=2AlN(s)+3CO(g) △H4=+1026kJ/mol
反应③的a=______,反应④自发进行的条件是______(填“高温”、“低温”或“任意温度”)
(2)在常压、Ru/TiO2催化下,CO2和H2混和气体(体积比1:4,总物质的量x mol)进行反应,测得CO2转化率、CH4和CO选择性随温度变化情况分别如图1和图2所示(选择性:转化的CO2中生成CH4或CO的百分比)。
反应ⅠCO2(g)+4H2(g)![]() CH4(g)+2H2O(g)△H4
CH4(g)+2H2O(g)△H4
反应ⅡCO2(g)+H2(g)![]() CO(g)+H2O(g)△H5
CO(g)+H2O(g)△H5
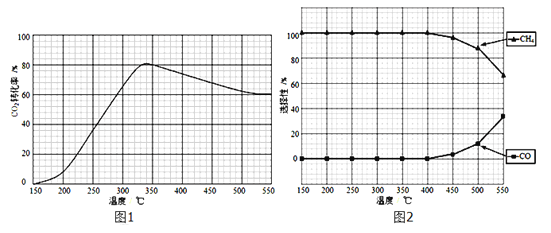
①下列说法正确的是___________。
A.△H5 小于零
B.温度可影响产物的选择性
C.CO2平衡转化率随温度升高先增大后减少
D.其他条件不变,将CO2和H2的初始体积比改变为1:3,可提高CO2平衡转化率
②350℃时,反应I在t1时刻达到平衡,平衡时容器体积为yL,该温度下反应I的平衡常数为____(用x、y 表示)。
(3)CO2溶于水形成H2CO3。已知常温下H2CO3 的电离平衡常数K1=4.4×10-7,K2=4.7×10-11,NH3·H2O的电离平衡常数Kb=1.75×10-5。常温下,用氨水吸收CO2 可得到NH4HCO3 溶液,NH4HCO3 溶液显______(填“ 酸 性”、“ 中性” 或“ 碱性”);请计算反应NH4++HCO3-+ H2O![]() NH3·H2O+H2CO3 的平衡常数K=_____________。
NH3·H2O+H2CO3 的平衡常数K=_____________。
(4)据文献报道,二氧化碳可以在酸性水溶液中用情性电极电解得到乙烯,其原理如图所示。
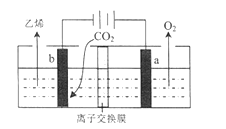
b电极上的电极反应式为____________________________,该装置中使用的是________(“ 阴”或“ 阳”) 离子交换膜。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E为原子序数依次增大的5种短周期主族元素,其中仅含有一种金属元素,A单质是自然界中密度最小的气体,A和D最外层电子数相同;B原子的最外层电子数是次外层电子数的两倍; C和E在周期表中相邻,且E的质子数是C的2倍。请回答下列问题:
(1)B位于第___周期___族;
(2)E的离子结构示意图是_____;DA中含有_______。(填化学键类型)
(3)BC2的电子式为________;(用具体元素表示,下同)
(4)C、D、E三种元素简单离子的离子半径由大到小的顺序是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若不断地升高温度,实现“雪花→水→水蒸气→氧气和氢气”的转化。在转化的各阶段被破坏的粒子间的主要相互作用依次是
A. 氢键;分子间作用力;非极性键
B. 氢键;氢键;极性键[
C. 氢键;极性键;分子间作用力
D. 分子间作用力;氢键;非极性键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com