
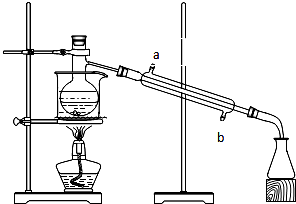
 实验题:如图所示的仪器装置,在蒸馏烧瓶中装有冰醋酸、乙醇、浓硫酸和沸石,水浴加热,粗制乙酸乙酯.反应一段时间后,将粗产品倒入装有水的烧杯中,液体分为两层,现用两种方法检验
实验题:如图所示的仪器装置,在蒸馏烧瓶中装有冰醋酸、乙醇、浓硫酸和沸石,水浴加热,粗制乙酸乙酯.反应一段时间后,将粗产品倒入装有水的烧杯中,液体分为两层,现用两种方法检验分析 (1)采用水浴加热,可以使液体受热均匀;浓硫酸在酯化反应中起到了催化剂和吸水剂的作用;
(2)冷凝管中采用逆向通水冷却效果好;
(3)乙酸乙酯的密度小于水的密度,据此判断乙酸乙酯的位置;根据碘易溶在有机物中分析;根据酸性高锰酸钾具有强氧化性,能氧化水中的乙醇分析;
(4)先用饱和碳酸钠溶液除去乙酸和乙醇,然后通过分液操作分离出乙酸乙酯.
解答 解:(1)反应需要加热,而采用水浴加热,可以使液体受热均匀;
因为反应是可逆反应,有水生成,水浴浓硫酸的作用是催化剂和吸水剂,
故答案为:使反应物受热均匀;催化剂、吸水剂;
(2)冷凝时逆向通水冷却效果好,所以应该从b口进水,
故答案为:b;
(3)乙酸乙酯的密度小于水的,所以在上层;因为碘易溶在有机物中,而上层呈紫红色,据此判断应该在上层;酸性高锰酸钾溶于具有强氧化性,能氧化水中的乙醇,所以颜色消失,
故答案为:上;上层液体呈紫红色;KMnO4氧化留在水层中的乙醇;
(4)要想得到乙酸乙酯,就需要除去挥发出的乙酸和乙醇,同时还不能减少乙酸乙酯,所以可利用饱和碳酸钠溶液,因为饱和碳酸钠可以吸收乙酸,溶解乙醇,同时降低乙酸乙酯的溶解度,最后通过分液即可,
故答案为:向粗制酯里加入饱和Na2CO3溶液,振荡后分液,分离出上层液即为纯净的酯.
点评 本题通过乙酸乙酯的制备,考查了制备方案的设计,题目难度中等,明确实验目的和实验原理为解答关键,注意掌握酯化反应原理及化学实验基本操作方法,试题培养了学生的分析能力及化学实验能力.


科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 将KI和FeCl3溶液在试管中混合后,滴加KSCN溶液 | 溶液变红色 | 氧化性:Fe2+>I2 |
| B | 少量的乙烯通入pH=3的溴水中 | 溴水褪色,pH基本不变 | 两者发生的加成反应 |
| C | 向某溶液中滴加稀NaOH溶液,将湿润红色石蕊试纸置于试管口 | 试纸不变蓝 | 溶液中一定无NH4+ |
| D | 等体积pH=3的HA和HB两种酸分别与足量的锌反应,排水法收集气体 | HA放出的氢气多且反应速率快 | HA酸性比HB强 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
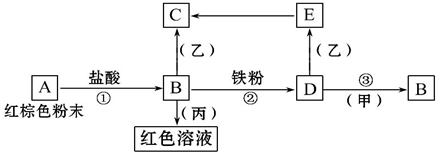 下列物质之间有如下反应关系,已知由E转化成C的现象是:灰白色沉淀迅速变为灰绿色,最后变为红褐色.
下列物质之间有如下反应关系,已知由E转化成C的现象是:灰白色沉淀迅速变为灰绿色,最后变为红褐色.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
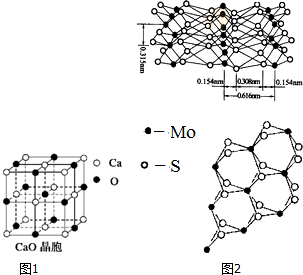 决定物质性质的重要因素是物质结构.请回答下列问题.
决定物质性质的重要因素是物质结构.请回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.3g钠由原子变成离子时,失去的电子数目为0.2NA | |
| B. | 0.2NA个硫酸分子与19.6g磷酸分子含有相同的氧原子数 | |
| C. | 28g氮气所含原子数为NA | |
| D. | NA个氧分子与NA个氢分子的质量比为2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 向新制的氯水中加KI?淀粉溶液即可证明 | |
| B. | 向久置失效的氯水中加KI?淀粉溶液即可证明 | |
| C. | 直接观察氯水溶液仍显黄绿色即可说明,不需进一步实验 | |
| D. | 用实验证明干燥的氯气不能使干燥的有色布条褪色,能使湿润的有色布条褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 规律 | 结论 |
| A | 溶解度小的沉淀易向溶解度更小的沉淀转化 | ZnS 沉淀中滴加CuSO4 溶液可以得到CuS 沉淀 |
| B | 较强酸可以制取较弱酸 | 次氯酸溶液无法制取盐酸 |
| C | 反应物浓度越大,反应速率越快 | 常温下,相同的铝片中分别加入足量的浓、稀硝酸,浓硝酸中铝片先溶解完 |
| D | 结构和组成相似的物质,沸点随相对分子质量增大而升高 | NH3的沸点低于PH3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将溴水加入苯中 | 溴水颜色变浅 | 苯与溴水发生取代反应 |
| B | 将SO2通入到Ba(NO3)2溶液中 | 有白色沉淀 | 沉淀成分为BaSO3 |
| C | 等体积、等PH的HA和HB两种溶液分别与足量的锌反应 | 相同时间内,HA酸产生的氢气多 | HA为强酸 |
| D | 将少量溴水加入KI溶液中,再加入CCl4,振荡,静置 | 下层液体呈紫色 | Br2的氧化性强于I2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com