
| 化学键 | Cl2 | Br2 | I2 | HCl | HBr | HI | H2 |
| 能量(kJ) | 243 | 193 | 151 | 432 | 366 | 298 | 436 |
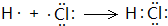 ;185
;185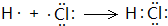 ,反应方程式为H2+Cl2=2HCl,反应生成2mol产物时释放的能量=2×432kJ-(436kJ+243kJ)=185kJ;(2)用离子方程式表示S、Cl两种元素的非金属性强弱为:Cl2+S2-=S↓+2Cl-,可以根据单质与氢气反应的难易程度及最高价氧化物对应水化物的酸性强弱比较非金属性强弱,单质沸点属于物理性质,不能比较非金属性强弱,故A错误,BC正确;(3)H、O、S形成的负一价双原子阴离子,且甲有18个电子,乙有10个电子,则甲为HS-,乙为OH-,离子反应为HS-+OH-=S2-+H2O。
,反应方程式为H2+Cl2=2HCl,反应生成2mol产物时释放的能量=2×432kJ-(436kJ+243kJ)=185kJ;(2)用离子方程式表示S、Cl两种元素的非金属性强弱为:Cl2+S2-=S↓+2Cl-,可以根据单质与氢气反应的难易程度及最高价氧化物对应水化物的酸性强弱比较非金属性强弱,单质沸点属于物理性质,不能比较非金属性强弱,故A错误,BC正确;(3)H、O、S形成的负一价双原子阴离子,且甲有18个电子,乙有10个电子,则甲为HS-,乙为OH-,离子反应为HS-+OH-=S2-+H2O。

 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案科目:高中化学 来源:不详 题型:单选题

| A.原子半径:W> Z>Y>X |
| B.最高价氧化物对应水化物的酸性:Z>W>X |
| C.4种元素的单质中,Z单质的熔、沸点最低 |
| D.W单质能与水反应,生成一种具有漂白性的物质 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| a | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | b | c | d | | |
| | e | | | | | | | | | | | f | | g | | | |
| | | | | | | | | h | I | | | | | | | | |
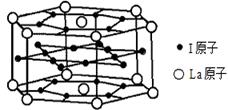
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.元素Y的最高化合价为+7 |
| B.三种元素的原子半径rZ>rY>rX |
| C.Z的单质比Y的单质更易与H2反应 |
| D.化合物X2Z2中阴阳离子数之比为1: 2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| | 氟 | 氯 | 溴 | 碘 |
| 第一电离能 (kJ/mol) | 1681 | 1251 | 1140 | 1008 |
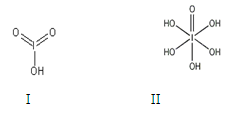


查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
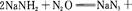
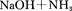
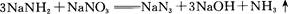 回答下列问题:
回答下列问题: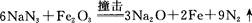
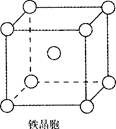
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
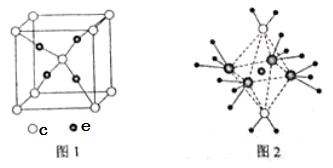
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
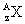 与
与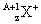 的两种微粒,下列叙述正确的是( )
的两种微粒,下列叙述正确的是( )| A.一定都是由质子、中子、电子组成的 |
| B.化学性质几乎完全相同 |
| C.核电荷数和核外电子数一定相等 |
| D.质子数一定相同,质量数和中子数一定不相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com