
| A. | 1 mol NH4+含有的电子数为11NA | |
| B. | NH4+中N元素的化合价为-3,在氧化还原反应中常作氧化剂 | |
| C. | 0.1 L 3 mol•L-1的NH4NO3溶液中氮原子数等于0.6NA | |
| D. | 硫酸铵中既含有离子键,又含有共价键,而氯化铵中只含有离子键 |
分析 A、铵根离子为10电子微粒;
B、-3价为氮元素的最低价态;
C、求出硝酸铵的物质的量m=CV,然后根据1mol硝酸铵中含2mol氮原子来分析;
D、铵根离子中N和H之间为共价键.
解答 解:A、铵根离子为10电子微粒,故1mol铵根离子中含10mol电子即10NA个,故A错误;
B、-3价为氮元素的最低价态,而元素的最低价只有还原性,故铵根离子在反应中常做还原剂,故B错误;
C、溶液中硝酸铵的物质的量m=CV=3mol/L×0.1L=0.3mol,而1mol硝酸铵中含2mol氮原子,故0.3mol硝酸铵中含0.6mol氮原子即0.6NA个,故C正确;
D、铵盐均为离子化合物.铵根离子中N和H之间为共价键,故硫酸铵和氯化铵中均既含离子键又含共价键,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
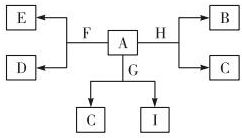 如图是中学化学某些物质之间的相互转化关系,已知A是种常见的液态化合物,C、D、G、H均为单质,G、H形成的合金是当前使用量最大的一种合金,B是黑色固体.
如图是中学化学某些物质之间的相互转化关系,已知A是种常见的液态化合物,C、D、G、H均为单质,G、H形成的合金是当前使用量最大的一种合金,B是黑色固体.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
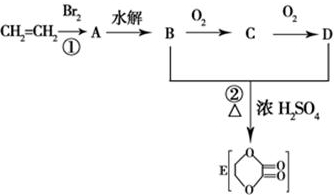
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
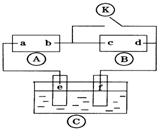 图中
图中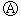 为直流电源,
为直流电源,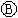 为浸透饱和氯化钠溶液和酚酞试液的滤纸,
为浸透饱和氯化钠溶液和酚酞试液的滤纸,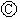 为电镀槽.接通电路后发现
为电镀槽.接通电路后发现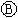 上的c点显红色.为实现铁上镀锌,接通
上的c点显红色.为实现铁上镀锌,接通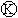 后,下列叙述正确的是( )
后,下列叙述正确的是( )| A. | a为直流电源的负极 | B. | d极发生的反应为2H++2e-═H2↑ | ||
| C. | e极发生氧化反应 | D. | f电极为锌板 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在常温常压下,71g Cl2所含原子数为NA | |
| B. | 标准状况下,22.4L氦气中含有的原子数为2NA | |
| C. | 在非标准状况下,1mol任何气体的体积不可能是22.4L | |
| D. | 常温常压下,32g O2和O3混合气体中含有原子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. |  分散系的分类 | B. | 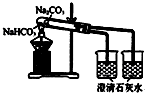 比较Na2CO3、NaHCO3的稳定性 | ||
| C. | 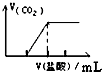 向Na2CO3溶液中逐滴滴入盐酸 | D. | 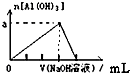 向Al溶液中滴加过量的NaOH溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com