
| A. | AlCl3═Al3++Cl- | B. | Ca(OH)2═Ca2++(OH)2- | ||
| C. | Mg(NO3)2═Mg2++2NO3- | D. | Na2SO4═Na2++SO42- |
分析 A.电离方程式中电荷不守恒;
B.氢氧根离子符号错误;
C.Mg(NO3)2电离出1个镁离子和2个硝酸根离子;
D.钠离子符号错误.
解答 解:A.电离方程式中电荷不守恒,所以电离方程式为AlCl3═Al3++3Cl-,故A错误;
B.氢氧根离子符号错误,则氢氧化钙的电离方程式为:Ca(OH)2═Ca2++2OH-,故B错误;
C.Mg(NO3)2电离出1个镁离子和2个硝酸根离子,则电离方程式为:Mg(NO3)2═Mg2++2NO3-,故C正确;
D.钠离子符号错误,硫酸钠的电离方程式为Na2SO4═2Na++SO42-,故D错误.
故选C.
点评 本题考查电离方程式的书写知识,注意强电解质在溶液中能完全电离,弱电解质部分电离,离子团在电离方程式中不能拆开,强酸的酸式根离子要拆开,弱酸的酸式根离子不能拆开,题目难度不大.


 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案 互动课堂系列答案
互动课堂系列答案科目:高中化学 来源: 题型:解答题
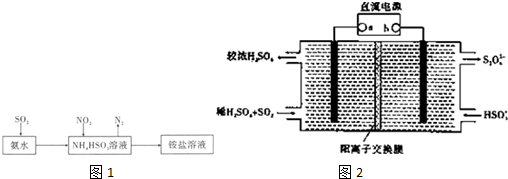
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ③④ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 豆腐、肉冻、果冻的生产 | B. | 工厂中设置的静电除尘装置 | ||
| C. | 河流入海口处三角洲的形成 | D. | 大气污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
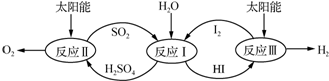
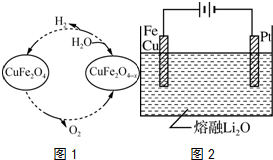
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
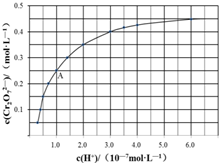 元素铬(Cr)在溶液中主要以Cr3+(蓝紫色)、Cr(OH)4-(绿色)、Cr2O72-(橙红色)、CrO42-(黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,回答下列问题:
元素铬(Cr)在溶液中主要以Cr3+(蓝紫色)、Cr(OH)4-(绿色)、Cr2O72-(橙红色)、CrO42-(黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com