
【题目】钴元素是三元锂离子电池阳极材料的重要成分。请回答下列问题:
(1)钴元素在周期表中的位置是______________。
(2)已知第四电离能大小:I4(Fe)> I4 (Co),从原子结构的角度分析可能的原因是__________。
(3)Cu2Cl22CO2H2O是一种配合物,其结构如图所示:
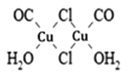
①该配合物中氯原子的杂化方式为______。
②该配合物中,CO作配体时配位原子是C而不是O的原因是______。
(4)某种铀氮化物的晶体结构是NaCl型。NaCl的Bom-Haber循环如图所示。已知:元素的一个气态原子获得电子成为气态阴离子时所放出的能量称为电子亲和能。下列有关说法正确的是__(填标号)。

a、Cl-Cl键的键能为119.6kJ/mol b、Na的第一电离能为603.4kJ/mol
c、NaCl的晶格能为785.6kJ/mol d、Cl的第一电子亲和能为348.3kJ/mol
(5)碲化锌晶体有两种结构,其中一种晶胞结构如图:

若与Zn距离最近的Te原子间距为a pm,则晶体密度为__________g/cm3。
【答案】第四周期Ⅷ Co失去的是3d6上的一个电子,而Fe失去的是半充满状态3d5上的一个电子,故Fe需要的能量较高 sp3 电负性C<O,C对孤电子对的吸引力较弱,更容易给出孤电子对 cd 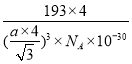
【解析】
根据原子的电子层数及其价电子数确定元素在周期表中的位置。根据原子及其离子的价电子排布分析其电离能的相对大小。根据价层电子对互斥理论分析原子的杂化类型。根据电负性的大小分析配合物中的配位原子。分析表中数据并结合相关概念判断有关变化中能量变化。根据晶胞结构分析晶体的化学式并进行相关计算。
(1)钴是27号元素,其有4个电子层,其价电子排布式为3d74s2,因此,其在周期表中的位置是第四周期Ⅷ族。
(2)Fe的价电子排布式为3d64s2,其失去3个电子后变为较稳定的半充满结构3d5,而Co的价电子排布式为3d74s2,其失去3个电子后变为3d6。因此,从原子结构的角度分析I4(Fe)> I4 (Co)的可能原因是:Co失去的是3d6上的一个电子,而Fe失去的是半充满状态3d5上的一个电子,故Fe需要的能量较高。
(3)由Cu2Cl22CO2H2O的结构 可知:
可知:
①该配合物中氯原子均形成2个σ键,另外每个氯原子还有2个孤电子对,故其价层电子对数为4,其杂化方式为sp3。
②CO分子中的C原子和O原子均有孤电子对,但是O元素的电负性大于C元素,故O原子对孤电子对的吸引力更强,因此,该配合物中,CO作配体时配位原子是C而不是O的原因是:电负性C<O,C对孤电子对的吸引力较弱,更容易给出孤电子对(用于形成配位键)。
(4)a、由图中信息可知,![]() Cl2(g)=Cl(g)的H=119.6kJ/mol,因此, Cl-Cl键的键能为239.2kJ/mol ,a不正确;
Cl2(g)=Cl(g)的H=119.6kJ/mol,因此, Cl-Cl键的键能为239.2kJ/mol ,a不正确;
b、由图中信息可知,Na(g)=Na+(g)+e-的H=495.0kJ/mol,因此, Na的第一电离能为603.4kJ/mol,b不正确;
c、由图中信息可知,Cl-(g)+ Na+(g)= NaCl(s)的H= -785kJ/mol,因此,NaCl的晶格能为785.6kJ/mol,c正确;
d、由图中信息可知,Cl(g) +e-=Cl-(g) 的H= -348.3kJ/mol,因此,Cl的第一电子亲和能为348.3kJ/mol,d正确。
综上所述,有关说法正确的是cd。
(5)由碲化锌晶体的晶胞结构示意图可知,其晶胞结构与金刚石相似,Te原子堆积方式为面心立方最密堆积,Zn距离最近的Te原子间距为体对角线长度的![]() ,高晶胞参数(即该晶胞的边长)为x,则晶胞的体对角线长度为,
,高晶胞参数(即该晶胞的边长)为x,则晶胞的体对角线长度为,![]() x=4a pm,故x=
x=4a pm,故x=![]() pm,晶胞的体积为x3=
pm,晶胞的体积为x3=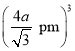 。该晶胞中占有4个Te原子和4个Zn原子,则晶胞的质量为
。该晶胞中占有4个Te原子和4个Zn原子,则晶胞的质量为![]() 。因此,该晶体密度为
。因此,该晶体密度为
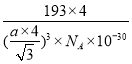 g/cm3。
g/cm3。


 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案 期末好成绩系列答案
期末好成绩系列答案科目:高中化学 来源: 题型:
【题目】某课外活动小组用如图装置进行实验,试回答下列问题:
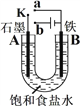
(1) 若开始时开关K与a连接,则A极的电极反应式为______________________________。
(2) 若开始时开关K与b连接,总反应的离子方程式为________________________________。
(3) 有关上述实验(2)的下列说法,正确的是(填序号)_________。
①溶液中Na+向A极移动
②从A极处逸出的气体能使湿润的KI淀粉试纸变蓝
③反应一段时间后加适量盐酸可恢复到电解前电解质的浓度
④若标准状况下B极产生2.24 L气体,则溶液中转移0.2 mol电子
(4) 该小组同学认为,如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。
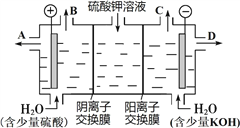
①该电解槽的阳极反应式为____________________________。
②制得的氢氧化钾溶液从出口(填“A”、“B”、“C”或“D”)______导出。
③若将甲醇和氢氧化钾溶液组合为甲醇燃料电池,则电池负极的电极反应式为_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第ⅤA族元素的原子R与A原子结合形成RA3气态分子,其立体结构呈三角锥形。RCl5在气态和液态时,分子结构如图所示,下列关于RCl5分子的说法中正确的是( )
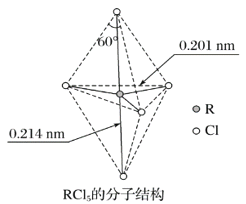
A. 每个原子都达到8电子稳定结构
B. 键角(Cl—R—Cl)有90°、120°、180°几种
C. RCl5受热后会分解生成分子RCl3,RCl5和RCl3都是极性分子
D. 分子中5个R—Cl键键能不相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列可设计成原电池的化学反应是( )
A. H2O(l)+CaO(s)=Ca(OH)2(s)
B. Ba(OH)2·8H2O+2NH4Cl=BaCl2+2NH3·H2O+8H2O
C. 2KClO3![]() 2KCl+3O2↑
2KCl+3O2↑
D. CH4(g)+2O2(g) ![]() CO2(g)+2H2O(l)
CO2(g)+2H2O(l)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各反应对应的离子方程式正确的是
A.向100 mL 0.12 mol·L1的Ba(OH)2溶液中通入0.02 mol CO2: Ba2++3OH+2CO2=![]() +BaCO3↓+H2O
+BaCO3↓+H2O
B.向Ca(OH)2溶液中加入过量的NaHCO3溶液:Ca2++2OH+2![]() =
=![]() CaCO3↓+
CaCO3↓+![]() +2H2O
+2H2O
C.硫酸氢钠与氢氧化钡两种溶液反应后溶液恰好呈中性:H++![]() +Ba2++OH=BaSO4↓+H2O
+Ba2++OH=BaSO4↓+H2O
D.向含0.1 mol NaOH和0.2molNa2CO3的溶液中加入1L0.4 mol·L1稀盐酸:OH+![]() +3H+=CO2↑+2H2O
+3H+=CO2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇、二甲醚(CH3OCH3) 既是重要的化工原料,又是可再生能源,具有开发和应用广阔前景。
(1)合成二甲醚的反应原理为2CO(g)+4H2(g)![]() CH3OCH3(g)+H2O(g)。
CH3OCH3(g)+H2O(g)。
①该反应能够自发进行的原因是_______。
②若容器的体积恒定不变,CO、H2起始通入量分别为2 mol、4 mol,充分反应后达到平衡。下列措施既可以提高反应速率又可以提高CO的转化率是_______。
a.升高温度 b.使用更高效的催化剂
c.充入He,使体系总压强增大 d.缩小体积增大压强
(2)工业上合成甲醇的化学方程式为CO(g)+2H2(g)![]() CH3OH(g) ΔH=-91 kJ·mol-1
CH3OH(g) ΔH=-91 kJ·mol-1
①已知某些化学键的键能数据如下表,则x=_______。
化学键 | C-H | H-H | C-O | C≡O | O-H |
键能/ kJ·mol-1 | a | b | c | x | d |
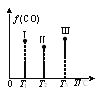
②在Ⅰ、Ⅱ、Ⅲ三个恒压容器中分别充入a mol CO和2a mol H2合成甲醇,三个容器的温度分别为T1、T2、T3。若实验测得反应均进行到t min时,三个容器中CO的体积分数如图所示,此时Ⅰ、Ⅱ、Ⅲ三个容器中一定达到化学平衡状态的是_____。若反应达到平衡,三个容器中v(CH3OH)逆最大的是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃煤烟气中含有大量的二氧化硫,进行脱硫处理可以减少环境污染,变废为宝。
(1)H2还原法是处理燃煤烟气中SO2的方法之一。已知:2H2S(g)+SO2(g)=3S(s)+2H2O(l) ΔH=a kJ·mol-1;H2S(g)=H2(g)+S(s) ΔH=b kJ·mol-1;H2O(l)=H2O(g) ΔH=c kJ·mol-1;写出SO2(g)和H2(g)反应生成S(s)和H2O(g)的热化学方程式:_______。
(2)新型纳米材料氧缺位铁酸盐(ZnFe2Ox)能使工业废气中酸性氧化物分解除去,若2 mol ZnFe2Ox与足量SO2可生成2 mol ZnFe2O4和1.0 mol S,则x=_______。
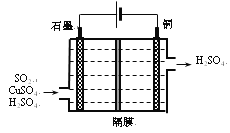
(3)一种以铜作催化剂脱硫有如下两个过程:
①在铜的作用下完成工业尾气中SO2的部分催化氧化,所发生反应为:2SO2+2n Cu+(n+1)O2+(2-2 n)H2O=2n CuSO4+(2-2n) H2SO4,吸收标准状况下11.2L SO2,被SO2还原的O2的质量为______g。
②利用如所示电化学装置吸收另一部分SO2,并完成Cu的再生。写出装置内所发生反应的离子方程式______;若用甲烷燃料电池作电源(电解质溶液呈碱性),负极的反应式为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】大马酮是一种主要用于高级化妆品和食品的香料,可通过以下方法合成:
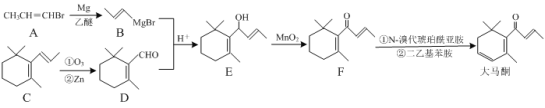
(1)E→F的反应类型为________。
(2)物质A具有顺反异构,写出A的顺式结构:_______。
(3)写出同时满足下列条件的大马酮的一种同分异构体的结构简式:_______。
①能发生银镜反应
②含有苯环,分子中有4种不同化学环境的氢
(4)请以![]() 为原料制备,写出制备
为原料制备,写出制备![]() 的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)________。
的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)________。
查看答案和解析>>
科目:高中化学 来源: 题型:
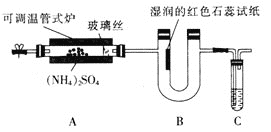
【题目】为了检验硫酸铵的热分解产物,某同学设计了如图所示实验装置。
回答下列问题:
(1)![]() 装置A中玻璃丝的作用是________。
装置A中玻璃丝的作用是________。
![]() 若在
若在![]() 时加热,B中湿润的红色石蕊试纸变蓝,则有________(填化学式
时加热,B中湿润的红色石蕊试纸变蓝,则有________(填化学式![]() 产生;若C中盛放
产生;若C中盛放![]() 溶液,有白色沉淀产生,________(填“能”或“不能”
溶液,有白色沉淀产生,________(填“能”或“不能”![]() 说明分解产物中有
说明分解产物中有![]() ,理由是________________;若要检验是否有
,理由是________________;若要检验是否有![]() 产生,C中应盛放的试剂是________。
产生,C中应盛放的试剂是________。
(2)若在A中装入![]() ,按下图连接,在
,按下图连接,在![]() 时加热至完全分解。
时加热至完全分解。
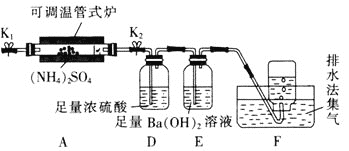
![]() 实验结束后,为防止倒吸,正确的操作是________。
实验结束后,为防止倒吸,正确的操作是________。
![]() 浓硫酸吸收的气体是________
浓硫酸吸收的气体是________![]() 填化学式
填化学式![]() 。
。
![]() 若D中增重
若D中增重![]() ,E中增重
,E中增重![]() ,F中收集的气体为
,F中收集的气体为![]() 已折算为标准状况
已折算为标准状况![]() ,分解反应的化学方程式为________。
,分解反应的化学方程式为________。![]() 已知分解产物中没有
已知分解产物中没有![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com