
【题目】大气污染越来越成为人们关注的问题,烟气中的NOx必须脱除(即脱硝)后才能排放.
(1)已知:CH4(g)+2O2(g)═CO2(g)+2H2O(1)△H=﹣890.3kJmol﹣1N2(g)+O2(g)═2NO(g)△H=+180kJmol﹣1
CH4可用于脱硝,其热化学方程式为:CH4(g)+4NO(g)=CO2(g)+2N2(g)+2H2O(1),△H= .
(2)C2H4也可用于烟气脱硝.为研究温度、催化剂中Cu2+负载量对NO去除率的影响,控制其它条件一定,实验结果如图1所示.为达到最高的NO去除率,应选择的反应温度和Cu2+负载量分别是 . 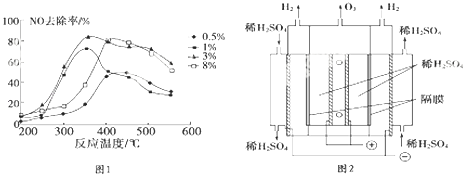
(3)臭氧也可用于烟气脱硝. ①O3氧化NO 结合水洗可产生HNO3和O2 .
②一种臭氧发生装置原理如图2所示.阳极(惰性电极)的电极反应式为 .
③将石墨电极设置成颗粒状的目的是 .
(4)如图3是一种用NH3脱除烟气中NO的原理. 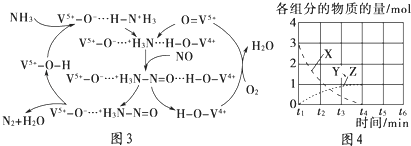
①该脱硝原理中,NO最终转化为(填化学式).
②当消耗2molNH3和0.5molO2时,除去的NO在标准状况下的体积为 .
(5)NO直接催化分解(生成N2与O2)也是一种脱硝途径.在不同条件下,NO的分解产物不同.在高压下,NO在40℃下分解生成两种化合物,体系中各组分物质的量随时间变化曲线如图4所示.写出Y和Z的化学式: .
(6)NO2会污染环境,可用Na2CO3溶液吸收NO2并生成CO2 . 已知9.2g NO2和Na2CO3溶液完全反应时转移电子0.1mol,此反应的离子方程式是;恰好反应后,使溶液中的CO2完全逸出,所得溶液呈弱碱性,则溶液中存在的所有离子浓度大小关系是c(Na+)> .
【答案】
(1)﹣1250.3 kJ?mol﹣1
(2)350℃左右、3%
(3)3H2O﹣6e﹣═O3↑+6H+;增大吸收液与电极的接触面积,提高电解反应的效率
(4)N2;44.8L
(5)N2O、NO2
(6)2NO2+CO32﹣=NO3﹣+NO2﹣+CO2;c(NO3﹣)>c(NO2﹣)>c(OH﹣)>c(H+)
【解析】解:(1)已知:①CH4(g)+2O2(g)═CO2(g)+2H2O(l);△H=﹣890.3kJmol﹣1②N2(g)+O2(g)═2NO(g);△H=+180kJmol﹣1根据盖斯定律:①﹣2×②得CH4(g)+4NO(g)═CO2(g)+2N2(g)+2H2O(l),△H=﹣890.3kJmol﹣1﹣2×(+180kJmol﹣1)=﹣1250.3 kJmol﹣1;
所以答案是:﹣1250.3 kJmol﹣1;(2)由图1可知在350℃左右,催化剂中Cu2+负载量为3%时,NO去除率最高;所以答案是:350℃左右、3%;(3)②酸性条件下,水在阳极失电子生成臭氧,生成1mol臭氧转移6mol电子,则电极方程式为:3H2O﹣6e﹣═O3↑+6H+;所以答案是:3H2O﹣6e﹣═O3↑+6H+;③将石墨电极设置成颗粒状的目的是,增大吸收液与电极的接触面积,提高电解反应的效率所以答案是:增大吸收液与电极的接触面积,提高电解反应的效率;(4)①由图3可知反应物为氧气、一氧化氮和氨气最终生成物为氮气和水,所以NO最终转化为N2和H2O;所以答案是:N2;②氧气、一氧化氮和氨气反应生成氮气和水,反应中氨气失去的电子的物质的量等于NO和氧气得到的电子总物质的量,2mol NH3转化为N2失去6mol电子,0.5mol O2得到2mol电子,则NO转化为N2得到的电子为4mol,所以NO的物质的量为2mol,其体积为44.8L;所以答案是:44.8L;(5)NO在40℃下分解生成两种化合物,根据元素守恒可知生成的为N的氧化物,氮元素的氧化物有NO、N2O、NO2、N2O3、N2O4、N2O5 , 由图象可知3molNO生成两种氮的氧化物各为1mol,其反应方程式为:3NO=Y+Z,根据原子守恒可知为N2O、NO2;所以答案是:N2O、NO2;(6)9.2gNO2的物质的量 ![]() =0.2mol,Na2CO3溶液完全反应生成CO2时转移电子0.1mol,反应中只有N元素化合价变化,则N的化合价分别由+4价变化为+5价和+3价,反应的离子方程式为:2NO2+CO32﹣=NO3﹣+NO2﹣+CO2 , 在碱性溶液中应生成NaNO3和NaNO2 , 二者浓度相等,NO2﹣水解溶液呈碱性,所得溶液中的离子浓度大小关系为c(Na+)>c(NO3﹣)>c(NO2﹣)>c(OH﹣)>c(H+),
=0.2mol,Na2CO3溶液完全反应生成CO2时转移电子0.1mol,反应中只有N元素化合价变化,则N的化合价分别由+4价变化为+5价和+3价,反应的离子方程式为:2NO2+CO32﹣=NO3﹣+NO2﹣+CO2 , 在碱性溶液中应生成NaNO3和NaNO2 , 二者浓度相等,NO2﹣水解溶液呈碱性,所得溶液中的离子浓度大小关系为c(Na+)>c(NO3﹣)>c(NO2﹣)>c(OH﹣)>c(H+),
所以答案是:2NO2+CO32﹣=NO3﹣+NO2﹣+CO2;c(NO3﹣)>c(NO2﹣)>c(OH﹣)>c(H+).
【考点精析】根据题目的已知条件,利用化学平衡状态本质及特征的相关知识可以得到问题的答案,需要掌握化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效).


科目:高中化学 来源: 题型:
【题目】实验室中需要配制2 mol·L-1的NaCl溶液950 mL,配制时应选用的容量瓶的规格和称取的NaCl质量分别是( )
A. 950 mL,111.2 g B. 500 mL,117.0 g
C. 1 000 mL,117.0 g D. 任意规格,111.2 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是分离混合物时常用的仪器,从左至右,可以进行的混合物分离操作分别是( )
A.蒸馏、蒸发、分液、过滤
B.蒸馏、过滤、分液、蒸发
C.分液、过滤、蒸馏、蒸发
D.过滤、蒸发、分液、蒸馏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 甲烷是最简单的有机化合物
B. 葡萄糖属于多糖,能发生水解
C. 油脂有油和脂肪之分,但都属于酯
D. 石油的分馏是物理变化,煤干馏是化学变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值,下列说法正确的是( )
A.常温常压下,17g NH3所含的电子数是 10NA
B.常温常压下,22.4L氧气含氧原子数为2NA
C.0.5 mol/L K2SO4溶液中含有NA个K+离子
D.2.3g金属钠与氧气反应全部生成Na2O时失去的电子数是0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温、容积为2L的密闭容器中充入2mol SO2和一定量O2 . 发生反应2SO2+O22SO3 , 当反应进行到4min时,测得n(SO2)=0.4mol.若反应进行到2min时,容器中SO2的物质的量是( )
A.等于1.6 mol
B.等于1.2 mol
C.大于1.6 mol
D.小于1.2 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2H2(g)+O2(g)═2H2O(l)△H=﹣571.6kJmol﹣12CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l)△H=﹣1452kJmol﹣1H+(aq)+OH﹣(aq)═H2O(l)△H=﹣57.3kJmol﹣1下列说法正确的是( )
A.H2(g)的燃烧热为571.6 kJ?mol﹣1
B.同质量的H2(g)和CH3OH(l)完全燃烧,H2(g)放出的热量多
C.![]() H2SO4(aq)+
H2SO4(aq)+ ![]() Ba(OH)2(aq)═
Ba(OH)2(aq)═ ![]() BaSO4(s)+H2O(l)△H=﹣57.3 kJ?mol﹣1
BaSO4(s)+H2O(l)△H=﹣57.3 kJ?mol﹣1
D.3H2(g)+CO2(g)=CH3OH(l)+H2O(l)△H=+135.9 kJ?mol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下关于水的说法正确的是:
A. 只饮用纯净水有益人体健康
B. 蒸馏水中不含任何离子
C. 明矾可作净水剂,除去水中的悬浮颗粒等杂质
D. 通过过滤的方法可将硬水软化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列基态原子的电子排布式中,其未成对电子数最多的是( )
A.1s22s22p63s23p63d54s1
B.1s22s22p63s23p3
C.1s22s22p63s23p63d64s2
D.1s22s22p63s23p63d74s2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com