
| A. | 漂白粉长期暴露在空气中最后会变质失效 | |
| B. | 对“地沟油”进行分馏可得到汽油 | |
| C. | PM2.5是对空气中直径小于或等于2.5微米(2.5×10-6m)的固体颗粒或液滴的总称,其分散在空气中一定形成气溶胶 | |
| D. | 氯气溶于水生成次氯酸有强氧化性,可以起净水和杀菌消毒的作用 |
分析 A.碳酸酸性强于次氯酸,漂白粉的有效成分次氯酸钙能够与二氧化碳反应;
B.地沟油主要成分为油脂,汽油成分为烃类;
C.胶体粒子的直径介于1nm~100nm之间;
D.氯水能够杀菌消毒,不能除去水中杂质.
解答 解:A.漂白粉长期暴露在空气中,其有效成分Ca(ClO)2会与空气中的CO2、H2O反应生成HClO,HClO分解使漂白粉变质失效,故A正确;
B.地沟油的主要成分是油脂,而汽油的主要成分是烃,所以对“地沟油”进行分馏不可能可得到汽油,故B错误;
C.胶体粒子的直径介于1nm~100nm(10-9m~10-7m)之间,PM2.5是指大气中直径≤2.5×10-6m的颗粒物,不一定为胶体,故C错误;
D.氯气溶于水生成次氯酸有强氧化性,可以起到杀菌消毒作用,但不能除去水中杂质,故D错误.
故选A.
点评 本题考查了漂白粉的性质、油脂的组成、胶体以及氯气的化学性质,题目难度中等,注意掌握氯水的性质及应用.


科目:高中化学 来源: 题型:多选题
| A. | CH3-CH2-CH3 | B. | CH2=CHCH2CH3 | C. | CH3C=CCH2CH3 | D. | 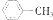 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 现象或事实 | 反应类型 |
| A | 四氯化碳和苯酚都能使溴水褪色 | 取代反应 |
| B | 甲苯和甲酸都能使酸性高锰酸钾溶液褪色 | 氧化反应 |
| C | 一氯甲烷和乙醇都能制备乙烯 | 消去反应 |
| D | 聚乙烯和聚乙炔都能使溴的四氯化碳溶液褪色 | 加成反应 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
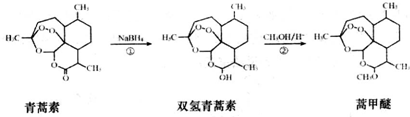
| A. | 青蒿素的分子式是C15H22O5,属于烃的衍生物 | |
| B. | 青蒿素难溶于水,而易溶于有机溶剂 | |
| C. | 反应②为取代反应,有H2O生成 | |
| D. | 青蒿素遇湿润的淀粉碘化钾试纸立刻显蓝色,是因为分子结构中含有酯基 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若X为氧化物,则Y也一定是氧化物 | |
| B. | 若M为金属单质,则N一定为金属单质 | |
| C. | 若X是不含金属元素的化合物,则N一定是非金属单质 | |
| D. | 若X是含有金属元素的化合物,则Y一定含有金属元素的化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若容积为某一固定值,当体系的压强不再发生变化时说明达到化学平衡状态 | |
| B. | 若上述可逆反应达化学平衡状态后,给平衡体系加压(缩小容积,其他条件不变),则容器内气体的平均摩尔质量将减小 | |
| C. | 若上述可逆反应达到化学平衡状态后,升高温度(其他条件不变)体系颜色加深,则Q>0 | |
| D. | 对于上述可逆过程给平衡体系减压(增大容积,其他条件不变),可以提高N2O4的产率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室可用浓硫酸干燥SO2气体 | |
| B. | 准确量取25.00 mL的液体可选用量筒或滴定管等量具 | |
| C. | 无色气体燃烧后生成的气体通入Ba(OH)2溶液,有白色沉淀生成,则原气体一定是CO | |
| D. | FeCl3、CuCl2的混合液中加铁粉充分反应后仍有固体存在,再加KSCN溶液可呈现血红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 利用黄花蒿叶研究青蒿素结构的基本步骤为:元素分析确定实验式→测定相对分子质量确定分子式→波谱分析确定结构式 | |
| B. | ①、②的反应类型分别为还原反应、酯化反应 | |
| C. | 双氢青蒿素在水中的溶解性大于青蒿素 | |
| D. | 双氢青蒿素与蒿甲醚组成上相差-CH2-,二者互为同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
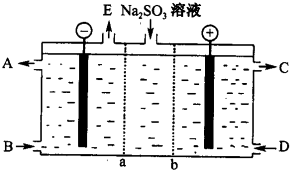
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com