
在室温下,某溶液中由水电离出的H+浓度为1.0×10-13 mol·L-1,则此溶液中一定不可能大量存在的离子组是ks5u
A.Mg2+、NO3-、Cl-、Na+ B.Al3+、SO42-、Cl-、K+
C.Na+、Fe2+、SO42-、NO3- D.S2-、SO32-、K+、Na+
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数的值。下列叙述正确的是
A.常温常压下,4.6g乙醇中含有C-H键的个数为0.6NA
B.一定温度下,15g甲醛和乙酸的混合物中O原子数为0.5NA
C.1mol Cl2和1mol H2O充分反应,生成的H+离子数为NA
D.标准状况下,11.2L庚烷完全燃烧后生成的CO2分子数为3.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
已知反应:2H2(g)+O2(g)=2H2O(l);△H= -571.6kJ·mol-1,下列对于反应2H2O(l)=2H2(g)+O2(g)的说法不正确的是
A.吸热反应 B.△S>0
C.只能在电解条件下进行 D.在一定温度下可以自发进行
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,某密闭容器中发生反应:2HI(g)  H2(g)+I2(g) △H>0,若15s内c(HI)由0.1 mol·L-1降到0.07 mol·L-1,则下列说法正确的是
H2(g)+I2(g) △H>0,若15s内c(HI)由0.1 mol·L-1降到0.07 mol·L-1,则下列说法正确的是
A.15s内用H2表示的平均反应速率为v(H2)=0.002 mol·L-1·s-1
B.升高温度平衡逆向移动
C.c(HI)由0.07 mol·L-1降到0.05 mol·L-1所需时间为10s
D.减小反应体系的体积,化学反应速率加快
查看答案和解析>>
科目:高中化学 来源: 题型:
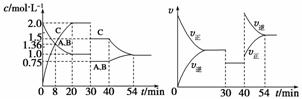
某密闭容器中充入等物质的量的A和B,一定温度下发生反应A(g)+xB(g)  2C(g),达到平衡后,在不同的时间段,分别改变影响反应的一个条件,测得容器中各物质的物质的量浓度、反应速率分别随时间的变化如下图所示:
2C(g),达到平衡后,在不同的时间段,分别改变影响反应的一个条件,测得容器中各物质的物质的量浓度、反应速率分别随时间的变化如下图所示:
下列说法中正确的是
A.30~40 min该反应使用了催化剂
B.反应方程式中的x=1,正反应为吸热反应
C.30 min时降低压强,40 min时升高温度
D.8 min时反应第一次达到平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
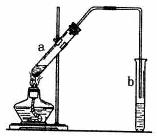
酯化反应是中学有机化学反应中重要的反应之一。右图为乙酸乙酯的制备装置图。a试管中装有适当过量的无水乙醇、2mL浓硫酸和2mL冰醋酸,小心均匀加热(避免副反应)至充分反应。请回答:
(1)写出反应的化学方程式 ▲ ;
(2)b试管中装的液体通常是 ▲ ,实验时往往在b试
管中可以看到少量气泡,写出与此现象对应的离子方程式 ▲ 。
(3)甲同学为了研究该反应机理使用了2H作同位素示踪原子。你认为合理吗?为什么?
▲ ;
乙同学采用“CH3CH218OH”做该实验,结果含18O原子的产物的结构简式为 ▲ ,乙酸分子中被取代的原子团的电子式为 ▲ ;
(4)浓硫酸在该反应中的作用是催化剂和 ▲ 剂,以此加快反应速率和 ▲ (用化学平衡知识答题)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液的滤纸。向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面。
己知:2KMnO4+16HCl=2KCl+5Cl2↑+2MnCl2+8H2O
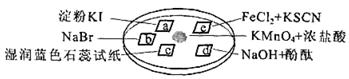
对实验现象的“解释或结论”正确的是
| 选项 | 实验现象 | 解释或结论 |
| A | a处变蓝,b处变红棕色 | 氧化性:Cl2>Br2>I2 |
| B | c处先变红,后褪色 | 氯气与水生成了酸性物质 |
| C | d处立即褪色 | 氯气与水生成了漂白性物质 |
| D | e处变红色 | 还原性:Fe2+ > Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
除去下列括号内杂质的试剂或方法错误的是( )
A、HNO3溶液(H2SO4),适量BaCl2溶液,过滤
B、Fe2+(Fe3+),还原铁粉,过滤
C、KNO3晶体(NaCl),蒸馏水,结晶
D、CO2(HCl),饱和NaHCO3溶液,洗气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com