
【题目】近年来,加“碘”食盐中较少使用碘化钾,因其口感苦涩且在贮藏和运输中易变化,目前代之加入是KIO_______(判断对错)。
科目:高中化学 来源: 题型:
【题目】砹(At)是卤族元素中位于碘后面的元素,试推测砹和砹的化合物最不可能具备的性质是
A. 砹易溶于某些有机溶剂 B. 砹化氢很稳定不易分解
C. 砹是有色气体 D. 砹化银不溶于水或稀HNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据海水综合利用的工业流程图(如下),判断下列说法正确的是
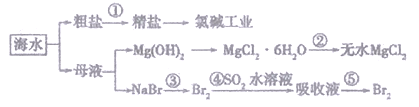
A. 从第③步到第⑤步的目的是为了富集
B. 在第②步中将MgCl2·6H2O灼烧即可制得无水MgCl2
C. 从能量转换角度看,氯碱工业中的电解饱和食盐水是一个将化学能转化为电能的过程
D. 除去粗盐中杂质(Mg2+、SO42-、Ca2+),加入的药品顺序为:NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T ℃时在2 L的密闭容器中X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的浓度变化如图1所示;若保持其他条件不变,反应温度分别为T1和T2时,Y的体积分数与时间的关系如图2所示。则下列结论正确的是
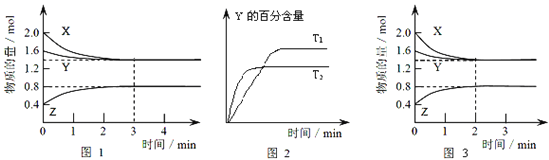 A.反应进行的前3 min内,用X表示的反应速率v(X)=0.3 mol·(L·min)-1
A.反应进行的前3 min内,用X表示的反应速率v(X)=0.3 mol·(L·min)-1
B.容器中发生的反应可表示为3X(g)+Y(g) ![]() 2Z(g)
2Z(g)
C.保持其他条件不变,升高温度,反应的化学平衡常数K减小
D.若改变反应条件,使反应进程如图3所示,则改变的条件是增大压强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列制取硫酸铜的实验设计中,能体现“经济、高效、环保”精神的最佳方案是( )。
A. 铜与浓硫酸共热
B. 用铜片为阳极,石墨为阴极,电解稀硫酸
C. 先灼烧废铜屑生成氧化铜,然后再用浓硫酸溶解
D. 适当温度下,使铜片在持续通入空气的稀硫酸中溶解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.1 L水中溶解了58.5 g NaCl,该溶液的物质的量浓度为1 mol/L
B.从1 L 2 mol/L的H2SO4溶液中取出0.5 L,该溶液的浓度为1 mol/L
C.配制480 mL 0.5 mol/L的CuSO4溶液,需62.5 g胆矾
D.10 g 98%的硫酸(密度为1.84 gcm﹣3)与10 mL18.4 molL﹣1的硫酸的浓度不同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com