
| 0.1×50+0.2×150 |
| 200 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、用分液的方法分离水和酒精的混合物 |
| B、容量瓶用水洗净后,可不经干燥直接用于配制溶液 |
| C、配制1L0.1mol/L的NaCl溶液时可用托盘天平称量5.85gNaCl固体 |
| D、用滴管滴加液体时,为防止液滴溅出,滴管紧贴试管内壁 |
查看答案和解析>>
科目:高中化学 来源: 题型:
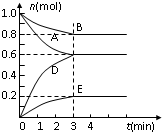 T℃、2L密闭容器中某一反应不同时刻各物质的量如图(E为固体,其余为气体).回答下列问题:
T℃、2L密闭容器中某一反应不同时刻各物质的量如图(E为固体,其余为气体).回答下列问题:| 物质 | A | B | D | E |
| 物质的量mol | 0.8 | 1.0 | 0.4 | 0.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 操作 | 现象 |
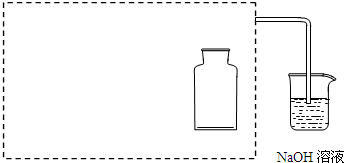
| a.用干燥洁净的烧杯取约10mL浓硝酸,加热. | / |
| b.把小块烧红的木炭迅速伸入热的浓硝酸中. | 红热的木炭与热的浓硝酸接触发生剧烈反应,同时有大量红棕色气体产生,液面上木炭迅速燃烧,发出光亮. |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| c(CH3COO-) |
| c(CH3COOH)?c(OH-) |
| c(CH3COOH) |
| c(CH3COO-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com