
| A、56g铁与足量的氯气反应,转移电子数为3NA |
| B、常温常压下,22.4L甲烷所含的电子数为10NA |
| C、常温常压下,34g氨气所含的原子数为8NA |
| D、NA个氧分子和NA个氢分子的质量比为16:1 |
| m |
| M |
| m |
| M |
| 34g |
| 17g/mol |


科目:高中化学 来源: 题型:
| A、负极发生的反应为:Fe-3e-=Fe3+ |
| B、正极发生的反应为:2H2O+O2+4e-=4OH? |
| C、原电池是将电能转变为化学能的装置 |
| D、钢铁在水下部分比在空气与水交界处更容易腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
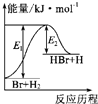
| A、该反应的△H=+(E1-E2)kJ?mol-1 |
| B、加入催化剂,该化学反应的反应热变大 |
| C、反应物的总能量高于生成物的总能量 |
| D、该反应为放热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、15g甲基(-CH3)所含有的电子数是10NA | ||
| B、0.5mol 1,3一丁二烯分子中含有的碳碳双键数为NA | ||
C、标准状况下,1 L戊烷充分燃烧后生成的气态产物的分子数为
| ||
| D、60gSiO2晶体中,含有NA个Si-O键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、制高铁酸钾用 KClO做还原剂 |
| B、Fe(OH)3是还原剂 |
| C、高铁酸钾中铁的化合价为+7 |
| D、制备高铁酸钾时1 molFe(OH)3得到3 mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HCO3-+H2O?H3O++CO32- |
| B、NH4++OH-?NH3?H2O |
| C、HSO3-+H2O?H2SO3+OH- |
| D、H2O+H2O?H3O++OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 测定序号 | 待测溶液的体积/mL | 所耗盐酸标准液的体积/mL | |
| 滴定前 | 滴定后 | ||
| 1 | 20.00 | 0.50 | 20.78 |
| 2 | 20.00 | 1.20 | 21.32 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
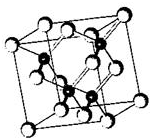 LED晶片在文化传媒中有着广泛的应用.目前市售LED晶片,材质基本以AlGaInP(磷化铝镓铟)、InGaN(氮化铟镓)为主.
LED晶片在文化传媒中有着广泛的应用.目前市售LED晶片,材质基本以AlGaInP(磷化铝镓铟)、InGaN(氮化铟镓)为主.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com