
| A. | ①②③⑤ | B. | ②③④⑤ | C. | 只有① | D. | ①② |
分析 SO2和CO2气体均为酸性氧化物,但二氧化硫具有漂白性、还原性,结合物质的性质差异及发生的反应来解答.
解答 解:①SO2和CO2气体都能与澄清石灰水反应生成沉淀,不能鉴别,故错误;
②使高锰酸钾褪色的为二氧化硫,无现象的为二氧化碳,可鉴别,故正确;
③使溴水褪色的为二氧化硫,无现象的为二氧化碳,可鉴别,故正确;
④酸化的Ba(NO3)2溶液与SO2发生氧化还原反应生成沉淀,而CO2不反应,故正确;
⑤使品红褪色的为二氧化硫,无现象的为二氧化碳,可鉴别,故正确.
则不能鉴别的为①.
故选C.
点评 本题考查物质的鉴别,为高频考点,把握物质的性质、性质差异及发生的反应等为解答的关键,侧重分析与应用能力的考查,注意二氧化硫的还原性,题目难度不大.


 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
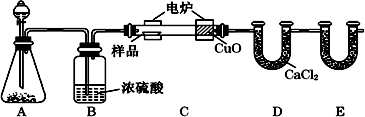
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
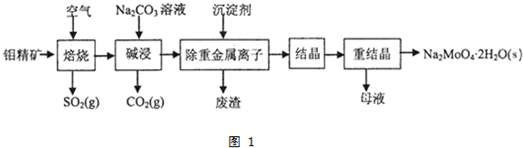
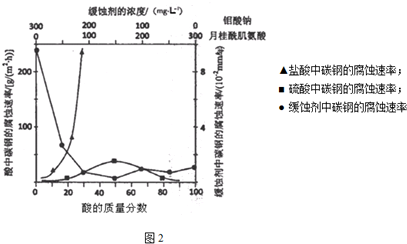
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 温度/℃ | 20 | 40 | 60 | 80 |
| 溶解度(Li2CO3)/g | 1.33 | 1.17 | 1.01 | 0.85 |
| 溶解度(Li2SO4)/g | 34.2 | 32.8 | 31.9 | 30.7 |

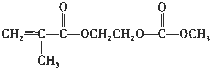 ,写出该单体与足量氢氧化钠溶液反应的化学方程式:
,写出该单体与足量氢氧化钠溶液反应的化学方程式: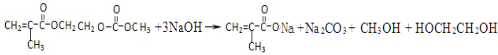 .
.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
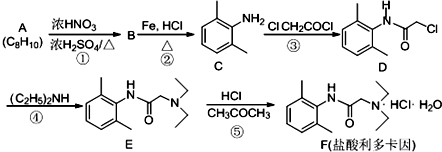
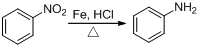
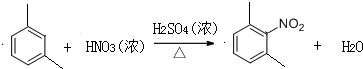 ,反应类型为取代反应,上述流程中,反应类型与①相同的还有③④(填反应序号).
,反应类型为取代反应,上述流程中,反应类型与①相同的还有③④(填反应序号). (R为烃基)
(R为烃基)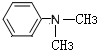 (写结构简式).
(写结构简式).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com