
| A. | ①② | B. | ①③ | C. | ①④ | D. | ②④ |
分析 ①碳酸氢钙与NaOH溶液反应中,氢氧化钠不足时生成碳酸钙沉淀、碳酸氢钠和水,氢氧化钠过量时生成碳酸钙沉淀、碳酸钠和水;
②苯酚钠溶液与二氧化碳反应生成苯酚和碳酸氢钠,与二氧化碳的量无关;
③氯气与氢氧化钠溶液反应生成氯化钠、次氯酸钠和水,与反应物是否过量无关;
④Fe与稀硝酸反应中,铁过量生成亚铁离子,铁不足生成铁离子.
解答 解:①碳酸氢钙与NaOH溶液反应中,碳酸氢钙与少量氢氧化钠溶液反应的离子反应为:Ca2++OH-+HCO3-═CaCO3↓+H2O,与过量氢氧化钠溶液反应的离子方程式为:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O,不能用同一个离子方程式表示,故①正确;
②苯酚的酸性大于碳酸氢根离子,为了二氧化碳是否过量,苯酚钠溶液与二氧化碳反应都生成苯酚和碳酸氢钠,反应的离子方程式为:C6H5O-+CO2+H2O→C6H5OH+NHCO3-,改变反应物用量,能用同一个离子方程式表示,故②错误;
③氯气与烧碱稀溶液反应的离子方程式为:Cl2+2OH-=Cl-+ClO-+H2O,改变反应物用量,能用同一个离子方程式表示,故③错误;
④Fe与稀硝酸反应,铁过量时的反应为:2NO3-+3Fe+8H+═3Fe2++2NO↑+4H2O,铁不足时生成铁离子,反应的离子方程式为:NO3-+Fe+4H+═Fe3++NO↑+2H2O,改变反应物用量,不能用同一个离子方程式表示,故④正确;
故选C.
点评 本题考查了离子方程式的书写,题目难度中等,侧重考查反应物用量对反应的影响,熟悉反应的实质是解题关键,注意掌握离子方程式的书写原则,试题有利于培养学生的灵活应用能力.


科目:高中化学 来源: 题型:选择题
| A. | c(NH4+)相等的NH4HCO3、NH4HSO4、NH4Cl三种溶液的物质的量浓度关系为c(NH4HSO4)>c(NH4HCO3)>c(NH4Cl) | |
| B. | 将10mL0.1mol•L-1Na2CO3溶液逐滴滴加到10mL0.1mol•L-1盐酸中:c(Na+)>c(Cl-)>c(HCO3-)>c(CO32-)>c(OH-) | |
| C. | 室温下,向100mL0.1mol/LNaOH溶液中滴加0.1mol/LNH4HSO4溶液至溶液呈中性,溶液中各离子浓度大小关系:c(Na+)>c(NH4+)>c(SO42-)>c(OH-)=c(H+) | |
| D. | 0.2mol•L-1的某一元弱酸HA溶液和0.1mol•L-1NaOH溶液等体积混合后的溶液:2c(OH-)+c(A-)═2c(H+)+c(HA) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
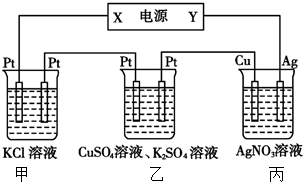
| A. | 当甲装置中共产生标准状况下4.48 L气体时,Cu电极上质量增加43.2g | |
| B. | 电解过程中装置丙的pH无变化 | |
| C. | 向甲中通人适量的HCl气体,可使溶液恢复到电解前的状态 | |
| D. | 乙中左侧电极反应式:Cu2++2e-=Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
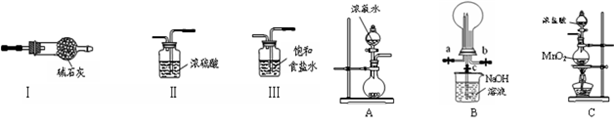
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓H2SO4有氧化性,稀H2SO4无氧化性 | |
| B. | 由于浓H2SO4具有脱水性,所以可用做干燥剂 | |
| C. | 稀H2SO4与铜不反应,但浓H2SO4在加热条件下可与铜反应 | |
| D. | 浓硫酸不与铁、铝发生钝化 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
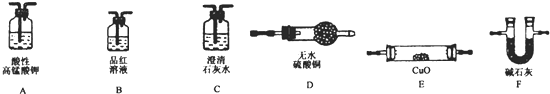
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H、Na、S、Cl、N | B. | H、Na、S、Br、P | C. | H、Li、O、F、N | D. | H、Mg、S、O、N |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl-的结构示意图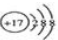 | B. | 氯化氢分子的电子式: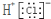 | ||
| C. | 碳-12原子${\;}_{5}^{12}C$ | D. | HClO的结构式H-O-Cl |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com