
3.2 g某元素A 的单质与氢气化合生成3.4 g气态氢化物H2A,已知A 的原子核中质子数和中子数相等,则:
(1) A的原子序数为?(2分)
(2) 元素A位于元素周期表中什么位置?(2分)
(3) 气态氢化物的化学式是什么?并书写气态氢化物的电子式(2分)
 全优点练单元计划系列答案
全优点练单元计划系列答案科目:高中化学 来源: 题型:
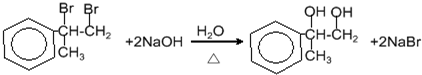
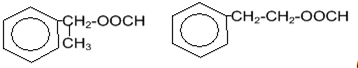
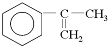 以为主要原理合成A的路线如下:
以为主要原理合成A的路线如下: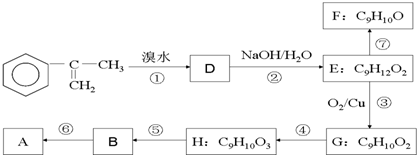



查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
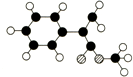
A是生产某新型工程塑料的基础原料之一,其组成元素为C、H、O,其分子结构模型如图所示(图中球与球之间连线代表化学键,不一定表示单键)。
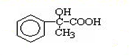
(1)根据分子结构模型写出A的结构简式______________________________。
(2)写出反应类型:反应①、⑤分别属于_______________、_______________。
(3)B与F均能与溴水中的溴发生加成反应,F的结构简式为______________________。
写出反应⑥的化学方程式(注明必要的反应条件)______________________________。
(4)已知G有多种芳香族同分异构体,其中符合下列条件的同分异构体共有___________种。
①能与稀硫酸及NaOH溶液反应
②能发生银镜反应
③分子中有一个甲基
查看答案和解析>>
科目:高中化学 来源:2013-2014学年湖北省武汉市高三二月调研测试理科综合化学试卷(解析版) 题型:填空题
已知X,Y,Z,Q为短周期非金属元素,R是长周期元素,X原子的电子占据2个电子层且原子中成对电子数是未成对电子数的2倍;Y的基态原子有7种不同运动状态的电子;Z元素在地壳中含量最多;Q是电负性最大的元素;R+离子只有三个电子层且完全充满电子。
回答下列问题:(答题时,X、Y、Z、Q、R用所对应的元素符号表示)
(1)X元素为???????? ,X、Y、Z中第一电离能最大的是???????? 。
(2)已知Y2Q2分子存在如图所示的两种结构(球棍模型,短线不一定代表单键):
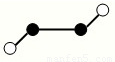
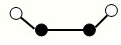
该分子中Y原子的杂化方式是???????? 。
(3)X与Y元素可以形成一种超硬新材料,其晶体部分结构如图所示,有关该晶体的说法正确的是???? (填正确答案编号)。

A.该晶体属于分子晶体
B.此晶体的硬度比金刚石还大
C.晶体的化学式是X3Y4
D.晶体熔化时破坏共价键
(4)有一种AB型分子与Y单质分子互为等电子体,它是一种常用的还原剂,其化学式为????????????? 。
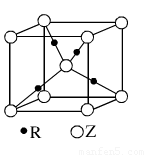
(5)R的基态原子的电子排布式为????????? ,R与Z形成的某离子晶体的晶胞结构如图,则该晶体的化学式为????????? ,该晶体的密度为a g·cm-3,则晶胞的体积是????????? cm3。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年福建省厦门市思明区双十中学高二(上)期中化学试卷(解析版) 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com