
下列表示方法错误的是 ( )
A. 氮分子的电子式: B. Cl—的离子结构示意图:
B. Cl—的离子结构示意图:
C. 甲烷分子的比例模型: D. 乙烯分子的球棍模型:
D. 乙烯分子的球棍模型:
 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案科目:高中化学 来源: 题型:
以“创新·未来”为主题的第十四届上海国际车展在浦东新国际博览中心举行。车展期间,新一代电动汽车因其“技术含量高”“节能环保”而倍受关注。液态锂离子电池是一种被采用的车载电池,该电池的电极反应如下:正极6C+xLi++xe-===LixC6,负极LiNiO2-xe-===Li1-xNiO2+xLi+。则有关该电池的下列说法中正确的是( )
A.放电时,电子从正极流向电源的负极
B.放电时,Li+向负极移动
C.该电池的总反应为LiNiO2+6C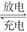 Li1-xNiO2+LixC6
Li1-xNiO2+LixC6
D.充电时,阳极发生的电极反应为Li1-xNiO2+xLi++xe-===LiNiO2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化学用语正确的是
A.乙醇的结构筒式:C2H6O
B.CH4的比例模型:
C.工业上制取粗硅的化学方程式: SiO2+C高温Si+CO2↑
D.电解饱和食盐水的离子方程式:2Cl-+2H2O===Cl2↑+2OH-+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
氧化铁在工业上具有广泛的应用。
I.据报道,一定条件下利用Fe2O3与甲烷反应可制取“纳米级”的金属铁。其反应如下:
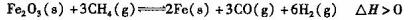
(1)若反应在2L的密闭容器中进行,5min后达到平衡,测得反应生成Fe的质量为l.12g。则该段时间内CH4的平均反应速率为 ________________ 。
(2)反应达到平衡后,保持其他条件不变,仅改变某一相关元素,下列说法正确的是 ________________(选填序号)。
a.若加入催化剂,v正增大,平衡向右移动
b.若温度升高,平衡常数K减小
c.若增大Fe2O3的量,平衡向右移动
d.若从反应体系中移走部分CO,可提高CH4的转化率
Ⅱ.工业上利用硫铁矿烧渣(主要成分为Fe2O3、A12O3、SiO2等)为原料提取Fe2O3,工艺 流程如下:试回答下列问题:
流程如下:试回答下列问题:
(3)结合下图,判断步骤ⅱ中调节溶液的pH范围_________________。
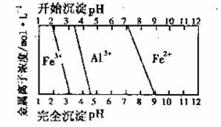
(4)写出步骤2中发生反应的离子方程式_____________________________,步骤2中分离出的滤渣的化学式是_________________。
(5)已知

 计算 的平衡常数为_____。
计算 的平衡常数为_____。
(6)在空气中煅烧FeCO3生成氧化铁的化学方程式为____________。
(7)结合所学化学知识,请你设计在实验室里从上述的硫铁矿烧渣中提取氧化铁的另一种简单方案_________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
醋酸和氢氧化钠溶液发生反应的离子方程式正确的是
A.H++OH-→H2O B.H++ NaOH→Na++H2O
C.CH3COOH +OH-→CH3COO- +H2O D.CH3COOH + NaOH→CH3COO-+ Na++H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
关于H2O2说法正确的是(NA代表阿伏加德罗常数) ( )
A.摩尔质量为34 g/mol B.每个H2O2分子含2NA个氧原子
C.2 mol H2O2含2 g氢元素 D.H2O2分子中H、O原子个数比为1:16
查看答案和解析>>
科目:高中化学 来源: 题型:
以色列科学家谢赫特曼因发现铝合金中的原子是以准晶体排列且硬度很高,而荣获诺贝尔奖。下列关于铝及其化合物的说法正确的是
A.铝元素比硅元素在地壳中的含量高
B.所有的铝合金遇浓硫酸、浓硝酸均能钝化
C.等质量的铝与足量的盐酸、氢氧化钠反应放出的氢气质量相等
D.等物质的量的明矾与Ba(OH)2反应的离子方程式为:
Al3++2SO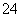 +2Ba2++4OH-===2BaSO4↓+AlO
+2Ba2++4OH-===2BaSO4↓+AlO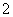 +2H2O
+2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com