
 合成氨工业对工、农业生产和国防都有重要意义.
合成氨工业对工、农业生产和国防都有重要意义.分析 (1)勒夏特列原理为:如果改变影响平衡的条件之一,平衡将向着能够减弱这种改变的方向移动,使用勒夏特列原理时,该反应必须是可逆反应,否则勒夏特列原理不适用;
(2)催化剂能降低反应所需活化能,能同等程度的增大正逆反应速率,缩短反应达到平衡状态的时间,但不引起平衡移动;
(3)先设氮气的转化率,再根据参加反应的氮气的量计算平衡时生成氨气的物质的量、剩余氮气的物质的量和剩余氢气的物质的量,再结合氨气的质量分数计算氨气的转化率.
解答 解:(1)a.用铁作催化剂加快化学反应速率,催化剂不能使平衡移动,使用催化剂是为了加快化学反应速率,用勒夏特列原理无法解释,故错误;
b.采用较高压强(20Mpa-50MPa),合成氨是气体体积减小的反应,加压至20~50MPa,有利于化学平衡正向移动,有利于氨的合成,故正确;
c.增大N2的浓度平衡正向移动,提高H2的转化率,故正确;
d.将生成的氨液化并及时从体系中分离出来,将氨及时液化分离,利于化学平衡正向移动,有利于氨的合成,故正确;
e.加热到500℃合成氨是放热反应,升温会使平衡逆向移动,降低转化率,升温的目的是为了保证催化剂的催化活性,加快化学反应速率,不能用勒夏特列原理解释,故错误;
故选bcd;
(2)催化剂能降低反应所需活化能,能同等程度的增大正逆反应速率,缩短反应达到平衡状态的时间,但不引起平衡移动,反应物和生成物总能量不变,所以其图象为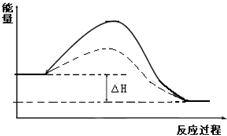 ,故答案为:
,故答案为: ;
;
(3)①设氮气的转化率是x.
N2 +3H2 ?2NH3
反应前0.2 0.8 0
反应 0.2x 0.6x 0.4x
平衡0.2(1-x)0.8-0.6x 0.4x
由题意可知:
$\frac{0.2+0.8}{1-0.4x}$x=50%,
故答案为:50%;
②所以N2的0.2(1-x)=0.1,H2 的0.8-0.6x=0.1;NH3的0.4x=0.2;所以
K1=$\frac{\frac{0.1}{2}×(\frac{0.1}{2})^{3}}{(\frac{0.2}{2})^{2}}$=12.8;答:平衡常数K1为12.8;
③若向该容积起始充入的N2、H2、NH3的量分别为0.1mol、0.6mol、0.2mol,Qc=$\frac{\frac{0.1}{2}×(\frac{0.6}{2})^{3}}{(\frac{0.2}{2})^{2}}$>K1,所以平衡正向移动,故答案为:正.
点评 本题考查化学平衡有关计算、化学平衡移动原理等知识点,为高频考点,侧重考查学生分析判断及计算能力,利用三段式法进行有关计算,易错点是平衡移动方向判断,题目难度不大.


 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案科目:高中化学 来源: 题型:解答题
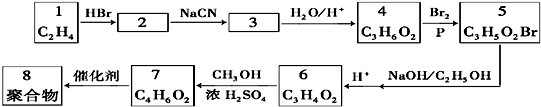

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH(NaOH) | B. | CuCl2(CuO) | C. | NaCl(HCl) | D. | CuSO4(H2O) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
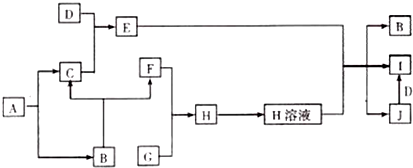
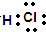 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| Y | Z | ||
| X | W |
| A. | 原子半径:X<Y<Z | |
| B. | 最高价氧化物的水化物的酸性:Y<W | |
| C. | 原子序数:X>W>Z>Y | |
| D. | Z、Y的单质均可与H2反应,且反应的剧烈程度:Y>Z |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C8H10中只有4种属于芳香烃的同分异构体 | |
| B. | CH3CH2CH2CH3光照下与氯气反应,生成2种一氯代烃 | |
| C. | 戊烷有3种同分异构体 | |
| D. | 甲苯苯环上的一个氢原子被-C3H7取代,所得产物有3种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②③ | C. | ②④ | D. | ①④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com