
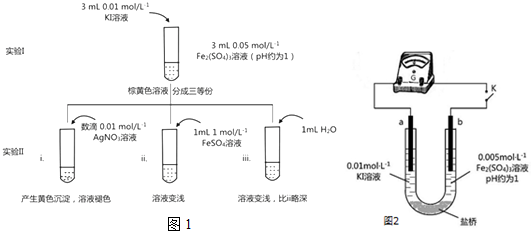
·ÖĪö £Ø1£©“żŹµŃéIČÜŅŗŃÕÉ«²»ŌŁøı䏱£¬ŌŁ½ųŠŠŹµŃéII£¬ÄæµÄŹĒŹ¹ŹµŃéIµÄ·“Ó¦“ļµ½»ÆŃ§Ę½ŗāדĢ¬£»
£Ø2£©øł¾ŻŹµŃéiiiŗĶŹµŃéiiµÄ¶Ō±ČæÉŅŌ擳öŹĒĪŖĮĖÅųżÓŠiiÖŠĖ®Ōģ³ÉČÜŅŗÖŠĄė×ÓÅضČøıäµÄÓ°Ļģ£»
£Ø3£©i£®¼ÓČėAgNO3£¬Ag+ÓėI-Éś³ÉAgI»ĘÉ«³Įµķ£¬I-ÅØ¶Č½µµĶ£¬2Fe3++2I-?2Fe2++I2Ę½ŗāÄęĻņŅĘ¶Æ£»
ii£®¼ÓČėFeSO4£¬Fe2+ÅضČŌö“ó£¬Ę½ŗāÄęŅĘ£»
¢ŁK±ÕŗĻŹ±£¬ÖøÕėĻņÓŅĘ«×Ŗ£¬æÉÖŖb¼«Fe3+µĆµ½µē×Ó£¬×÷Õż¼«£»
¢Śµ±ÖøÕė¹éĮć£Ø·“Ó¦“ļµ½Ę½ŗā£©ŗó£¬ĻņUŠĶ¹Ü×ó¹ÜÖŠµĪ¼Ó0.01mol/L AgNO3ČÜŅŗ£¬ČōÉś³É»ĘÉ«³Įµķ£¬æÉÖŖI-ÅØ¶Č½µµĶ£¬2Fe3++2I-?2Fe2++I2Ę½ŗāÄęĻņŅĘ¶Æ£»
£Ø5£©¢ŁFe2+ÅضČŌö“󣬻¹ŌŠŌŌöĒ棻
¢ŚÓė£Ø4£©ŹµŃé¶Ō±Č£¬²»Ķ¬µÄ²Ł×÷ŹĒµ±ÖøÕė¹éĮć£Ø·“Ó¦“ļµ½Ę½ŗā£©ŗó£¬ĻņUŠĶ¹ÜÓŅ¹ÜÖŠµĪ¼Ó0.01mol/L FeSO4ČÜŅŗ£»
£Ø6£©½«£Ø3£©ŗĶ£Ø4£©”¢£Ø5£©×÷¶Ō±Č£¬æÉÖŖŃõ»ÆŠŌ”¢»¹ŌŠŌÓėÅضČÓŠ¹Ų£®
½ā“š ½ā£ŗ£Ø1£©“żŹµŃéIČÜŅŗŃÕÉ«²»ŌŁøı䏱£¬ŌŁ½ųŠŠŹµŃéII£¬ÄæµÄŹĒŹ¹ŹµŃéIµÄ·“Ó¦“ļµ½»ÆŃ§Ę½ŗāדĢ¬£¬·ńŌņøÉČÅĘ½ŗāŅĘ¶ÆµÄÅŠ¶Ļ£¬
¹Ź“š°øĪŖ£ŗ»ÆŃ§Ę½ŗāדĢ¬£»
£Ø2£©ÓÉŹµŃéiiiŗĶŹµŃéiiµÄ¶Ō±ČæÉÖŖ£¬¶Ō±ČŹµŃéµÄÄæµÄŹĒĪŖĮĖÅųżÓŠiiÖŠĖ®Ōģ³ÉČÜŅŗÖŠĄė×ÓÅضČøıäµÄÓ°Ļģ£¬
¹Ź“š°øĪŖ£ŗČÜŅŗĻ”ŹĶ¶ŌŃÕÉ«µÄ±ä»Æ£»
£Ø3£©i£®¼ÓČėAgNO3£¬Ag+ÓėI-Éś³ÉAgI»ĘÉ«³Įµķ£¬I-ÅØ¶Č½µµĶ£¬2Fe3++2I-?2Fe2++I2Ę½ŗāÄęĻņŅĘ¶Æ£¬æÉÖŖFe2+ĻņFe3+×Ŗ»Æ£¬
¹Ź“š°øĪŖ£ŗAg+ÓėI-Éś³ÉAgI»ĘÉ«³Įµķ£¬I-ÅØ¶Č½µµĶ£¬2Fe3++2I-?2Fe2++I2Ę½ŗāÄęĻņŅĘ¶Æ£»
ii£®¼ÓČėFeSO4£¬Fe2+ÅضČŌö“ó£¬Ę½ŗāÄęŅĘ£»
¢ŁK±ÕŗĻŹ±£¬ÖøÕėĻņÓŅĘ«×Ŗ£¬ÓŅ²ąĪŖÕż¼«£¬æÉÖŖb¼«Fe3+µĆµ½µē×Ó£¬Ōņb×÷Õż¼«£¬
¹Ź“š°øĪŖ£ŗÕż£»
¢Śµ±ÖøÕė¹éĮć£Ø·“Ó¦“ļµ½Ę½ŗā£©ŗó£¬ĻņUŠĶ¹Ü×ó¹ÜÖŠµĪ¼Ó0.01mol/L AgNO3ČÜŅŗ£¬ČōÉś³É»ĘÉ«³Įµķ£¬I-ÅØ¶Č½µµĶ£¬2Fe3++2I-?2Fe2++I2Ę½ŗāÄęĻņŅĘ¶Æ£¬ÖøÕėĻņ×óĘ«×Ŗ£¬Ņ²æÉÖ¤Ć÷ĶĘ²āFe2+ĻņFe3+×Ŗ»Æ£¬
¹Ź“š°øĪŖ£ŗ×ó¹Ü³öĻÖ»ĘÉ«³Įµķ£¬ÖøÕėĻņ×óĘ«×Ŗ£»
£Ø5£©¢Ł×Ŗ»ÆµÄŌŅņĪŖFe2+ÅضČŌö“󣬻¹ŌŠŌŌöĒ棬Ź¹Fe2+»¹ŌŠŌĒæÓŚI-£¬
¹Ź“š°øĪŖ£ŗFe2+ÅضČŌö“󣬻¹ŌŠŌŌöĒ棬Ź¹Fe2+»¹ŌŠŌĒæÓŚI-£»
¢ŚÓė£Ø4£©ŹµŃé¶Ō±Č£¬²»Ķ¬µÄ²Ł×÷ŹĒµ±ÖøÕė¹éĮć£Ø·“Ó¦“ļµ½Ę½ŗā£©ŗó£¬ĻņUŠĶ¹ÜÓŅ¹ÜÖŠµĪ¼Ó0.01mol/L FeSO4ČÜŅŗ£¬Fe2+ĻņFe3+×Ŗ»Æ£¬
¹Ź“š°øĪŖ£ŗĻņUŠĶ¹ÜÓŅ¹ÜÖŠµĪ¼Ó0.01mol/L FeSO4ČÜŅŗ£»
£Ø6£©½«£Ø3£©ŗĶ£Ø4£©”¢£Ø5£©×÷¶Ō±Č£¬µĆ³öµÄ½įĀŪŹĒøĆ·“Ó¦ĪŖæÉÄęµÄŃõ»Æ»¹Ō·“Ó¦£¬ŌŚĘ½ŗāŹ±£¬ĶعżøıäĪļÖŹµÄÅØ¶Č£¬æÉŅŌøıäĪļÖŹµÄŃõ»Æ”¢»¹ŌÄÜĮ¦£¬²¢Ó°ĻģĘ½ŗāŅĘ¶Æ£¬
¹Ź“š°øĪŖ£ŗøĆ·“Ó¦ĪŖæÉÄęµÄŃõ»Æ»¹Ō·“Ó¦£¬ŌŚĘ½ŗāŹ±£¬ĶعżøıäĪļÖŹµÄÅØ¶Č£¬æÉŅŌøıäĪļÖŹµÄŃõ»Æ”¢»¹ŌÄÜĮ¦£¬²¢Ó°ĻģĘ½ŗāŅĘ¶Æ£®
µćĘĄ ±¾ĢāĪŖ2015Äź±±¾©øßæ¼ÕęĢā£¬²ąÖŲŌµē³Ų”¢Ńõ»Æ»¹Ō·“Ó¦¼°Ę½ŗāŅĘ¶ÆµÄ×ŪŗĻ漲飬°ŃĪÕĘ½ŗāŅĘ¶ÆµÄÓ°ĻģŅņĖŲ¼°ĪļÖŹµÄŠŌÖŹĪŖ½ā“šµÄ¹Ų¼ü£¬¶Ō·ÖĪöÓėŹµŃéÄÜĮ¦ŅŖĒó½Ļøߣ¬ĢāÄæÄŃ¶Č½Ļ“ó£®


 ĆūŹ¦µć²¦¾ķĻµĮŠ“š°ø
ĆūŹ¦µć²¦¾ķĻµĮŠ“š°ø Ó¢²Å¼Ę»®ĘŚÄ©µ÷ŃŠĻµĮŠ“š°ø
Ó¢²Å¼Ę»®ĘŚÄ©µ÷ŃŠĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
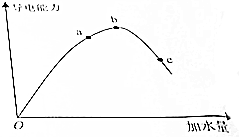 ŌŚŅ»¶ØĪĀ¶ČĻĀ£¬±ł“×Ėį¼ÓĖ®Ļ”ŹĶ¹ż³ĢÖŠ£¬ČÜŅŗµÄµ¼µēÄÜĮ¦ČēĶ¼ĖłŹ¾£¬Ēė»Ų“š£ŗ
ŌŚŅ»¶ØĪĀ¶ČĻĀ£¬±ł“×Ėį¼ÓĖ®Ļ”ŹĶ¹ż³ĢÖŠ£¬ČÜŅŗµÄµ¼µēÄÜĮ¦ČēĶ¼ĖłŹ¾£¬Ēė»Ų“š£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ė®·Ö×ÓÖŠ¹²¼Ū¼ü±ČĀČ»ÆÄĘÖŠĄė×Ó¼üČõ | |
| B£® | Ė®µÄĻą¶Ō·Ö×ÓÖŹĮæ±ČĀČ»ÆÄʵĊ” | |
| C£® | Ė®·Ö×Ó¼äÓŠ·¶µĀ»ŖĮ¦£¬ĀČ»ÆÄĘ·Ö×Ó¼äµÄ×÷ÓĆĮ¦½ĻĒæ | |
| D£® | Ė®·Ö×Ó¼äŹĒŅŌ·¶µĀ»ŖĮ¦Ļą½įŗĻ£¬Ļą»„×÷ÓĆ½ĻČõ£»ĀČ»ÆÄĘ¾§ĢåÖŠ£¬Na+ŗĶCl-ŅŌĄė×Ó¼üĻą½įŗĻ£¬×÷ÓĆĮ¦½ĻĒæ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ļ”ĻõĖįÖŠ¼ÓČė¹żĮæĢś·Ū£ŗFe+4H++NO${\;}_{3}^{-}$ØTFe3++NO”ü+2H2O | |
| B£® | ĻņNH4HSO4ČÜŅŗÖŠÖšµĪµĪČėBa£ØOH£©2ČÜŅŗÖĮĒ”ŗĆ³ĮµķĶźČ«2OH-+Ba2++2H++SO${\;}_{4}^{2-}$ØT2H2O+BaSO4”ż | |
| C£® | ĻņŃĒĮņĖį±µ¹ĢĢåÖŠ¼ÓČėĻ”ĻõĖį£ŗ3BaSO3+2H++2NO${\;}_{3}^{-}$ØT3BaSO4”ż+2NO”ü+H2O | |
| D£® | ĻņCa£ØClO£©2ČÜŅŗÖŠĶØČė×ćĮæCO2£ŗCa2++CO2+H2OØTCaCO3”ż+2H+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Na+”¢SO${\;}_{3}^{2-}$”¢SO${\;}_{4}^{2-}$”¢K+ | B£® | Na+”¢Cu2+”¢Br-”¢Ba2+ | ||
| C£® | K+”¢MnO${\;}_{4}^{-}$”¢NO${\;}_{3}^{-}$”¢Na+ | D£® | K+”¢Ca2+”¢SO${\;}_{3}^{2-}$”¢Cl- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŹÆ»ŅŹÆ | B£® | Ca£ØOH£©2 | C£® | CaCO3 | D£® | CH4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
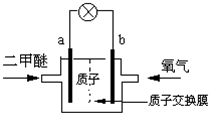 ŠĀÄÜŌ“æŖ·¢ÖŠµÄČ¼ĮĻµē³ŲŹĒµĶĢ¼ŃŠ¾æµÄÖŲŅŖĮģÓņ£®
ŠĀÄÜŌ“æŖ·¢ÖŠµÄČ¼ĮĻµē³ŲŹĒµĶĢ¼ŃŠ¾æµÄÖŲŅŖĮģÓņ£®²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com