
| A. | x=0.3a,2Fe2++Cl2→2Fe3++2Cl- | |
| B. | x=0.7a,2Br-+Cl2→Br2+2Cl- | |
| C. | x=1.2a,2Fe2++2Br-+2Cl2→Br2+2Fe3++4Cl- | |
| D. | x=1.5a,2Fe2++4Br-+3Cl2→2Br2+2Fe3++6Cl- |
分析 Fe 2+ 的还原性比Br- 强,所以Cl 2 通入FeBr 2 溶液中,当Cl 2 不足量时,会先与Fe 2+ 反应;待Fe 2+ 全部被氧化成Fe 3+ 后,过量的Cl 2 才会与Br- 反应,由此分析解答.
解答 解:由于还原性:Fe2+>Br-,通入Cl2,依次发生2Fe2++Cl2=2Fe3++2Cl-,2Br-+Cl2=Br2+2Cl-,
当n(Cl2):n(FeBr2)≤$\frac{1}{2}$时,只氧化Fe2+,
当n(Cl2):n(FeBr2)≥$\frac{3}{2}$时,Fe2+和Br-被完全氧化,介于二者之间时,Fe2+被完全氧化,Br-被部分氧化,则
A.x=0.3a,n(Cl2):n(FeBr2)=0.3<$\frac{1}{2}$,只氧化Fe2+,故A正确;
B.x=0.7a,n(Cl2):n(FeBr2)介于$\frac{1}{2}$~$\frac{3}{2}$,Fe2+被完全氧化,Br-被部分氧化,故B错误;
C.x=1.2a,n(Cl2):n(FeBr2介于$\frac{1}{2}$~$\frac{3}{2}$,Fe2+被完全氧化,Br-被部分氧化,则反应的离子方程式为10Fe2++14Br-+12Cl2=7Br2+10Fe3++24Cl-,故C错误;
D.x=1.5a,Fe2+和Br-恰好被完全氧化,反应的离子方程式为2Fe2++4Br-+3Cl2=2Br2+2Fe3++6Cl-,故D正确;
故选:BC.
点评 本题考查了离子方程式书写,侧重考查氧化还原反应离子方程式书写,明确氧化还原反应先后规律,熟悉溴离子、二价铁离子氧化性强弱关系是解题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 利用CO2合成聚碳酸酯可降解塑料,实现“碳”的循环利用 | |
| B. | 氯水中加入稀硫酸,可增强氯水的漂白性 | |
| C. | 用蘸有浓氨水的玻璃棒检验输送氯气的管道是否漏气 | |
| D. | 加工后具有吸水性的植物纤维可用作食品干燥剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
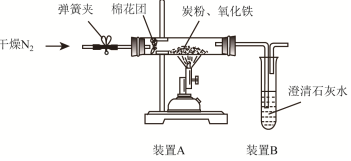
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有Fe2+和Cu2+ | B. | 一定有Fe2+、Cu2+,可能有Fe3+ | ||
| C. | 一定有Fe2+,可能有Cu2+ | D. | 只有Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 其原子核内有8个中子 | B. | 是C60的同素异形体 | ||
| C. | 是14N的同素异形体 | D. | 与C60互为同位素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石墨 | B. | 二氧化锰 | C. | 汞 | D. | 锌 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com