
 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:
设NA代表阿伏加德罗常数,下列说法不正确的是( )。
A.14g氮气所含原子数为NA
B.1 mol 水中所含电子数为10NA
C.32g O2与32g O3所含原子数分别为2NA和3NA
D.0.5mol Na2CO3与1.5mol H2O所含氧原子数目均为1.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
|
| A. | 氢氧化钠的摩尔质量是40g |
|
| B. | 1molNaOH的质量是40g/mol |
|
| C. | 1gH2和1gN2所含分子数相等 |
|
| D. | 阿伏伽德罗常数个钠原子的质量是23g |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式正确的是( )
A、利用醋酸溶解含碳酸钙的水垢:CaCO3+2H+===Ca2++H2O+CO2↑
B、用铜为电极电解饱和食盐水:2Cl-+2H2O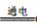 Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
C、在明矾溶液中滴加过量氨水:Al3++4NH3·H2O=AlO2-+4NH4++2H2O
D、在小苏打溶液中加少量 Ba(OH)2 溶液:2HCO3-+Ba2++2OH-=BaCO3↓+2H2O+CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的 pH 在 5.0~6.0 之间,通过电解生成 Fe(OH)3 沉淀。Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用。阴极产生的气泡把污水中悬浮物带到水面形成 浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用。某科研小组用电浮选凝聚法处理污水,设计装置如图所示: (1)实验时若污水中离子浓度较小,导电能力较差,产生气泡速率缓慢,则无法使悬浮物形成浮渣。

此时,应向污水中加入适量的_________。
a. H2SO4 b.BaSO4 c.Na2SO4 d.NaOH e.CH3CH2OH
(2)电解池阳极的电极反应分别是①______________;
②4OH--4e-=2H2O+O2↑
(3)电极反应①和②的生成物反应得到 Fe(OH)3 沉淀的离子方程式是__________。
(4)熔融盐燃料电池是以熔融碳酸盐为电解质,以 CH4为燃料,空气为氧化剂,稀土金属材料为电极。已知负极的电极反应是 CH4+4CO2-8e-===5CO2+2H2O。
①正极的电极反应是______________。
②为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定。为此电池工作时必须有部分A物质参加循环。 则 A 物质的化学式是___________。
(5)实验过程中,若在阴极产生了 44.8L(标准状况)气体,则熔融盐燃料电池消耗 CH4_____L(标准状况)。
查看答案和解析>>
科目:高中化学 来源: 题型:
10 g含有杂质的CaCO3和足量的盐酸反应,产生CO2 0.1 mol,则此样品中可能含有的杂质是( )。
A.KHCO3和MgCO3 B.MgCO3和SiO2 C.K2CO3和SiO2 D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
设计实验证明酸性强弱顺序:HCl>H2CO3>H2SiO3。
(1)写出实验原理的化学反应方程式________________。
(2)设计本实验所依据的化学原理是________________。
(3)实验中必须用到的药品有________________,所需的实验仪器有________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)将碳酸钙、稀盐酸、铁、氧气四种物质填写到下图的适当位置。

(2)从(1)中的四种物质中选出一种或几种为反应物,按下述反应类型,各写一个化学方程式。
①分解反应:__________________________________________。
②化合反应:__________________________________________。
③置换反应:__________________________________________。
④复分解反应:__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
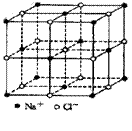
食盐晶体如图所示。在晶体中,· 表示Na+,o 表示Cl-。已知食盐的密度为r g / cm3,NaCl摩尔质量M g / mol,阿伏加德罗常数为N,则在食盐晶体里Na+和Cl-的间距大约是
 |
A. 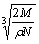 cm B.
cm B. 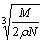 cm
cm
C. 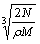 cm D.
cm D. 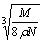 cm
cm
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com