
Ϊ�˳�ȥFeSO4��Һ�е�Fe3�������ü��봿��м�����˷��ܷ�ʱ������һ�ַ�����������ˮ����ʱ�����δ״���̷���������Σ������裬ֱ���۲쵽�к�ɫ������������ֹͣ����ҩƷ�����1��2���ӣ����ȹ��ˣ��ܷⱣ�����õ�FeSO4��Һ���˷���ԭ����
A��Fe3����ˮ�⣬����ˮ�����֮һ�����Ƶ�Fe2�� ˮ��
B��Fe2�� �н�ǿ�Ļ�ԭ�ԣ����ܻ�ԭFe3��
C��Fe3���н�ǿ�������ԣ���������Fe2��
D��Fe3����ˮ�������ȷ�Ӧ�������ܴٽ�����ˮ��
 ���źþ���Ԫ����ĩ��ϵ�д�
���źþ���Ԫ����ĩ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015������ʡ��������������У��һ��ѧ����ĩ������ѧ�Ծ��������棩 ���ͣ�ѡ����
�������з�Ӧ�ж��йص����ʻ�ԭ����ǿ������˳����
H2SO3+I2+H2O=2HI+H2SO4��2FeCl3+2HI=2FeCl2+2HCl+I2��3FeCl2+4HNO3=2FeCl3+NO��+2H2O+Fe(NO3)3
A��H2SO3��I-��Fe2+��NO B��I-��Fe2+��H2SO3��NO
C��Fe2+��I-��H2SO3��NO D��NO��Fe2+��H2SO3��I-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015������ʡ�߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���б�����ȷ����
A���� 0.1 mol��L��1HCl��Һ���ȵ�100�棬��Һ��pH��Ϊ1
B����pH��4�Ĵ�����Һ��ˮϡ�ͺ���Һ���������ӵ�Ũ�Ⱦ�����
C�������£���1mLpH��1��������10mLNaOH��Һ��Ϻ���Һ��pH=7����NaOH��Һ��pH=12
D���ڵ��з�̪��Һ�İ�ˮ�У�����NH4Cl����Һ����ɫ����ʱ��Һһ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015������ʡ�߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����������ڵ���ʵ���
A������ B���Ȼ��� C���������� D��ͭ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���Ϻ���ʮ��У�����ڶ���������ѧ�Ծ��������棩 ���ͣ������
�£�N2H4���ֳ���������Һ���ȼ��ȼ���Ƚϴ���ȼ�ղ���Ի�������Ⱦ�������������ȼ�ϡ�������ˮ��һ�ֶ�Ԫ�
���������գ�
��1��д���µĵ���ʽ ���µľ������� ��
��2����ҵ�Ͽ��ô������ƺͰ���Ӧ���£���ֻ��һ���������д���÷����Ʊ��µĻ�ѧ����ʽ ��
��3��0.2molҺ̬����������Һ̬˫��ˮ��Ӧ�����ɵ�����ˮ�������ų�128.3kJ��������
д���÷�Ӧ���Ȼ�ѧ����ʽ ��
��4�������£�N2H5Cl��ˮ��Һ�� �����ᡢ��У��ԡ�
��ԭ���ǡ�
��֪��H2O 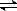 H + + OH- Kw = 1��10-14
H + + OH- Kw = 1��10-14
N2H4 + H2O 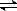 [N2H5]+ + OH- K1 = 8.5��10-7
[N2H5]+ + OH- K1 = 8.5��10-7
[N2H5]+ + H2O 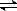 [N2H6]2++ OH- K2 = 8.4��10-15
[N2H6]2++ OH- K2 = 8.4��10-15
��5���¿��Ժ�������ӦN2H4��O2��N2��2H2O��Ϊ��ȥ��ѹ��¯��ˮ���ܽ��O2������N2H4��Na2SO3����ȥ�����ʵ�����O2�������ĵ�N2H4��Na2SO3������֮��Ϊ ��
��N2H4��Ƚϣ�ʹ��Na2SO3��Թ�¯��ɲ�����Ӱ�죬��ԭ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���Ϻ���ʮ��У�����ڶ���������ѧ�Ծ��������棩 ���ͣ�ѡ����
�����Լ�ʻԱ�Ƿ����ƽ��м���þƾ�����������ԭ���Ǿƾ���CrO3��Ӧ��������ɫ��Cr3����������ɫ�仯���ж��Ƿ������Ƽ��������Ķ��١����ж��Ҵ����ʵ�������˲ⶨԭ���ص���
A���е�� B���ܶȱ�ˮС C������ˮ D�����л�ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���Ϻ���ʮ��У�����ڶ���������ѧ�Ծ��������棩 ���ͣ�ѡ����
�����ƣ�Na3N����������ʱ�ܵ��硣����������ȷ����
A�����ɾ�������������Ӳ�ṹ��ͬ
B�����ɾ�����������뾶���
C�����ɾ�����������ĺ������������ͬ
D�����ɾ�����������ĵ��Ӳ�����ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�걱����˳����������һ��ͳһ��ϰ��ѧ�Ծ��������棩 ���ͣ�ѡ����
���ۻ������ؿ���Ϊҩ���������Ƽ��Ե�����Ⱦ�����Ը��ȼ�������ṹ��ʽ���¡����жԼ��ۻ������ص�����������ȷ����

A�����ۻ������ؿ��Է�����ȥ��Ӧ
B��1 mol���ۻ������ؿ��� 6 mol H2 �����ӳɷ�Ӧ
C�����ۻ������ؿ��� NaOH ��Һ�ڼ��������·���ˮ�ⷴӦ
D�����ۻ������ؼ�����Na��Ӧ����H2��������NaHCO3��Ӧ����CO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�긣��ʡ����4������������ۻ�ѧ�Ծ��������棩 ���ͣ������
�ۻ�ѧ�����ʽṹ�����ʡ���13�֣��衢�ࡢ�����������ء��۱�ϩ�����ǰ뵼����ϡ�
��1����̬�ࣨGe)ԭ�ӵĺ�������Ų�ʽΪ ��
��2���۱�ϩ���ɱ�ϩ����CH2��CH��CN���ۺ϶��ɡ���ϩ������������ԭ�Ӷ���ͬһƽ���ϣ����ϩ�������У�̼ԭ�ӵ��ӻ���������� �� �ĸ�����Ϊ ��
�ĸ�����Ϊ ��
��3����CH3)3Ga��(CH3CH2)3Ga����ȡ�����ڵij�����Դ�����³�ѹ�¾�Ϊ��ɫ����Һ�塣����˵����ȷ���� �����ţ���
A.��CH3��3Ga�������ڷ��Ӿ���
B.��CH3��3Ga��������ѧ�����Ǽ��Լ�
C.��CH3CH2��3Ga����������
D.��CH3CH2��3Ga������ԭ�Ӷ��ﵽϡ��������ȶ��ṹ
��4�������ڣ�GaN���ľ���ṹ������ͼ��ʾ���þ����� ����С����ޡ�����λ�����ڣ��жϵ�������
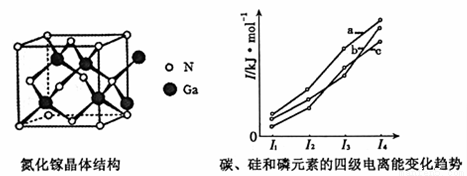
��5����ͼ��ʾ̼�������Ԫ�ص��ļ������ܱ仯���ƣ����б�ʾ�������� �����ţ���
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com