
观察下列几个装置示意图,有关叙述正确的是( )
|
| A. | 装置①中阳极上析出红色固体 |
|
| B. | 装置②的待镀铁制品应与电源正极相连 |
|
| C. | 装置③闭合电键后,外电路电子由a极流向b极 |
|
| D. | 装置④的X电极是外接电源的正极 |
| 原电池和电解池的工作原理.. | |
| 专题: | 电化学专题. |
| 分析: | A、电解池的阳极是电解质中的阴离子失电子的过程; B、根据电镀原理来回答判断; C、在燃料电池中,电子从负极流向正极; D、和电源正极相连的电极是阳极,阳极金属易被氧化. |
| 解答: | 解:A、装置①中阳极上是电解质中的氯离子失电子生成氯气的过程,故A错误; B、在电镀池中,镀件金属应该做阴极,镀层金属做阳极,故B错误; C、装置③闭合电键后,形成燃料电池,通氢气的极是负极,同氧气的极是正极,电子从负极流向正极,即由a极流向b极,故C正确; D、装置④中,和电源正极X相连的电极铁是阳极,阳极铁易被氧化而腐蚀,达不到防腐蚀的目的,故D错误. 故选C. |
| 点评: | 本题考查学生原电池和电解池的工作原理知识,可以根据教材知识来回答,注意平时知识的积累是解题的关键,难度中等. |


 新编小学单元自测题系列答案
新编小学单元自测题系列答案 字词句段篇系列答案
字词句段篇系列答案科目:高中化学 来源: 题型:
某蓝色电解质溶液中,只可能大量存在有Ag+、H+、Cu2+、CO32—、OH—、Cl—中的某些离子,你认为一定有的离子是 ,一定没有的离是 ,还需进一步确认的是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列事实均能说明醋酸是弱电解质的是
①醋酸与水能以任意比互溶 ②醋酸溶液能导电 ③醋酸溶液中存在醋酸分子 ④0.1 mol/L醋酸溶液的pH比0.1 mol/L盐酸的pH大 ⑤醋酸能和碳酸钙反应放出CO2 ⑥大小相同的锌粒与相同物质的量浓度的盐酸和醋酸溶液反应,开始醋酸产生H2速率慢
A.②③⑥ B.④⑤⑥ C.③④⑥ D.①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
100mL 浓度为2mol•L﹣1的盐酸跟过量的锌片反应,为加快反应速率,又基本不影响生成氢气的总量,可采用的方法是( )
|
| A. | 加入适量的6mol•L﹣1的盐酸 | B. | 加入数滴氯化铜溶液 |
|
| C. | 加入适量蒸馏水 | D. | 加入适量的氯化钠溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
Cu2O是一种半导体材料,基于绿色化学理念设计的制取.Cu2O的电解池如图,电解总反应:2Cu+H2O=Cu2O+H2↑.下列说法正确的是( )
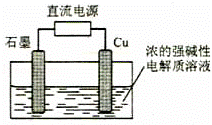
|
| A. | 当有0.1mol电子转移时,有0.1molCu2O生成 |
|
| B. | 铜电极发生还原反应 |
|
| C. | 铜电极接直流电源的负极 |
|
| D. | 石墨电极上产生氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
对于A+2B(g)⇌nC(g),在一定条件下达到平衡后,改变下列条件,请回答:
(1)A量的增减,平衡不移动,则A为 固或液 态.
(2)增大压强,平衡不移动,当n=2时,A为 固或液 态;当n=3时,A为 气 态.
(3)若A为固态,增大压强,C的组分含量减少,则n >2 .
(4)升温,平衡向右移动,则该反应的逆反应为 放热 热反应.
查看答案和解析>>
科目:高中化学 来源: 题型:
某无色溶液能与铝反应放出氢气,则该溶液中肯定不能大量共存的离子组是 ( )
A.NH4+、Na+、Ba2+、Cl- B.Na+、I-、HCO3-、SO42-
C.K+、Cl-、SO32-、AlO2- D.Na+、Mg2+、SO42-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
NA代表阿伏伽德罗常数,下列叙述正确的是
A.10 mL质量分数为98%的H2SO4,用水稀释至100 mL,H2SO4的质量分数为9.8%
B.1molFe与过量的稀HNO3反应,转移的电子数为2 NA
C.标准状况下,分子数为NA的CO、C2H4混合气体体积约为22.4 L,质量为28 g
D.一定温度下,l L 0.50 mol/LNH4C1溶液与2 L0.25mol/LNH4C1溶液NH4+的离子数均为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
按照物质的树状分类法和交叉分类法,对于H2SO4的分类正确的是( )
①酸 ②氧化物 ③氢化物 ④强酸 ⑤含氧酸
⑥难挥发性酸 ⑦一元酸 ⑧化合物 ⑨混合物
A.①④⑤⑥⑧ B.①②④⑤⑥⑦⑧ C.①③④⑤⑥⑨ D.①④⑤⑥⑦⑨
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com