
| 容器编号 | 起始时各物质物质的量/mol | 达平衡时体系能量的变化 | ||
| X2 | Y2 | XY3 | ||
| ① | 1 | 3 | 0 | 放热23.15kJ |
| ② | 0.6 | 1.8 | 0.8 | Q(Q>0) |
| A、容器①、②中反应的平衡常数相等 |
| B、达平衡时,两个容器中XY3的物质的量浓度均为2mol?L-1 |
| C、容器②中反应达到平衡时放出的热量为Q |
| D、若将容器①体积缩小为0.20L,则达平衡时放出的热量大于23.15kJ |
| 23.15kJ |
| 92.6kJ/mol |
| 0.5mol |
| 0.25L |
| 23.15kJ |
| 92.6kJ/mol |


 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案科目:高中化学 来源: 题型:
| A、无色溶液:Ca2+、H+、Cl-、HSO3- | ||
B、
| ||
| C、Na2CO3溶液:K+、Na+、SO42--、AlO2- | ||
| D、能使PH试纸呈红色的溶液:Na+、NH4+、I-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、电离程度:HCN>HClO |
| B、pH:HClO>HCN |
| C、NaOH恰好完全反应时,消耗NaOH的物质的量:HClO>HCN |
| D、酸根离子浓度:c(ClO-)>c(CN--) |
查看答案和解析>>
科目:高中化学 来源: 题型:
 我国节能减排“十二五规划”要求到2015年,全国二氧化碳排放总量控制在2086.4万吨.若能回收二氧化碳,其对工农业生产中有重要的作用.下列关于干冰(如图)的说法正确的是( )
我国节能减排“十二五规划”要求到2015年,全国二氧化碳排放总量控制在2086.4万吨.若能回收二氧化碳,其对工农业生产中有重要的作用.下列关于干冰(如图)的说法正确的是( )| A、干冰是弱电解质 |
| B、金属着火可以用干冰灭火 |
| C、氧碳两种元素可以组成不同的氧化物 |
| D、干冰在常温常压下稳定存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、②③ | C、③④ | D、①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
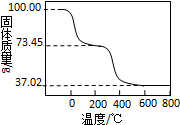 碱式碳酸铝镁[MgxAly(OH)a(CO3)b?nH2O]可做为塑料填料.为确定某碱式碳酸铝镁的组成,进行如下实验:
碱式碳酸铝镁[MgxAly(OH)a(CO3)b?nH2O]可做为塑料填料.为确定某碱式碳酸铝镁的组成,进行如下实验:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com