
【题目】除去下列物质中的杂质,所用试剂和方法正确的是( )
选项 | 物质 | 杂质 | 除杂质所用试剂和方法 |
A | KCl溶液 | I2 | CCl4,萃取 |
B | KNO3 | K2SO4 | BaCl2溶液,过滤 |
C | Fe | Cu | 稀硫酸,过滤 |
D | CaCO3 | CaO | 稀盐酸,过滤 |
A. A B. B C. C D. D
科目:高中化学 来源: 题型:
【题目】为了除去粗盐中的CaCl2、MgSO4及泥沙,可将粗盐溶于水,然后进行下列5项操作:①过滤;②加过量的NaOH溶液;③加适量盐酸;④加过量Na2CO3溶液;⑤加过量的BaCl2溶液。正确的操作顺序是()
A.①④②⑤③
B.④①②⑤③
C.②④⑤①③
D.⑤②④①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼及其化合物在工农业生产中应用广泛.
(1)基态硼原子的核外电子排布式为 , 有种不同能量的电子.
(2)BF3溶于水后.在一定条件下可转化为H3O+[B(OH)F3]﹣ , 该物质中阳离子的空间构型为 , 阴离子的中心原子轨道采用杂化.
(3)与BH4﹣互为等电子休的分子是(写化学式).
(4)EminBF4的熔点为12℃,在常温下为液体,由有机物阳离子[Emin]+和[BF4]﹣构成.该物质的晶体属于晶体.
(5)一种由硼和钐(Sm)形成的晶体的晶胞结构如图所示,已知晶胞常数a=n pm,则晶体的密度为gcm﹣3(设NA为阿伏伽德罗常数的值). 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏伽德罗常数的值.下列说法正确的是( )
A.n(H2CO3)和c(HCO3﹣)之和为1mol的NaHCO3溶液中,含有Na+数目为NA
B.5g 21H和31H的混合物发生热核聚变反应:21H+31H→42He+10n,净产生的中子(10n)数为NA
C.1L 0.1mol/L乙醇溶液中存在的共价键总数为0.8NA
D.56g 铁与足量氯气反应,氯气共得到3NA个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】准确称取6.0 g铝土矿样品(主要成分为Al2O3,含Fe2O3杂质),加入100 mL稀硫酸中,充分反应后向滤液中加入10 mol·L-1NaOH溶液,产生沉淀的质量和加入NaOH溶液体积之间的关系如图所示。则所用硫酸物质的量浓度为( )

A. 3.50 mol·L-1
B. 1.75 mol·L-1
C. 0.85 mol·L-1
D. 无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NO2是大气污染物之一,实验室拟用NO2与Cl2混合用NaOH溶液吸收的方法消除其污染.回答下列问题:
(1)氯气的制备 
①仪器M、N的名称依次是 .
②欲用MnO2和浓盐酸制备并收集一瓶纯净干燥的氯气,选呢图1中的装置,其连接顺序为(按气流方向,用小写字母表示).
③D在制备装置中的作用是;用离子方程式表示装置F的作用是 .
(2)用如图2所示装置探究Cl2和NO2在NaOH溶液中的反应. 查阅有关资料可知:HNO3是一种弱酸,且不稳定,易分解生成NO和NO2 .
①装置中X和Z的作用是
②实验时观察到X试剂瓶中有黄绿色气体,Z试剂瓶中有红棕色气体,若通入适当比例的Cl2和NO2 , Y中观察不到气体颜色,反应结束后加入稀硫酸无现象,则Y中发生反应的化学方程式是 .
③反应结束后,取Y中溶液少许于试管中,加入稀硫酸,若有红棕色气体产生,解释产生该现象的原因: . 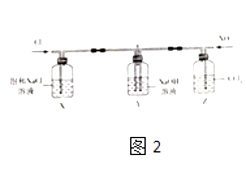
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷化铜(Cu3P2)用于制造磷青铜、磷青铜是含少量锡、磷的铜合金,主要用作耐磨零件和弹性原件.
(1)基态铜原子的电子排布式为;价电子中成对电子数有个.
(2)磷化铜与水作用产生有毒的磷化氢(PH3). ①PH3分子中的中心原子的杂化方式是 .
②P与N同主族,其最高价氧化物对应水化物的酸性:HNO3H3PO4(填“>”或“<”),从结构的角度说明理由: .
(3)磷青铜中的锡、磷两元素电负性的大小为SnP(填“>”“<”或“=”).
(4)某磷青铜晶胞结构如图所示. 
①则其化学式为 .
②该晶体中距离Cu原子最近的Sn原子有个,这些Sn原子所呈现的构型为 .
③若晶体密度为8.82g/cm3 , 最近的Cu原子核间距为pm(用含NA的代数式表示).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份。向其中一份中逐渐加入 铜粉,最多能溶19.2 g(已知硝酸只被还原为NO气体)。向另一份中逐渐加入铁 粉,产生气体的量随铁粉质量增加的变化如下图所示。下列分析或结果不正确的是( )

A. 图中,AB段的反应为Fe+2Fe3+===3Fe2+,溶液中溶质最终为硫酸亚铁
B. 原溶液中硫酸浓度为2.5 mol·L-1
C. 原混合溶液中硝酸根离子的物质的量为0.4 mol
D. 图中,OA段产生的气体是一氧化氮,BC段产生的气体是氢气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com