
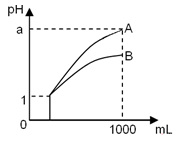
| A.物质的量浓度c(甲)=c(乙) |
| B.甲中由水电离产生的H+的物质的量浓度是乙的0.1倍 |
| C.中和等物质的量浓度等体积的NaOH溶液需甲、乙两酸的体积V(乙)=10V(甲) |
| D.甲中的c(OH-)为乙中c(OH-)的10倍 |
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
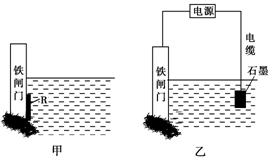
| A.铜 | B.钠 | C.锌 | D.石墨 |
 http://photo.blog.sina.com.cn/showpic.html - blogid=515359c40100g2ml&url=http://static3.photo.sina.com.cn/orignal/515359c4g79a1c1001942&690
http://photo.blog.sina.com.cn/showpic.html - blogid=515359c40100g2ml&url=http://static3.photo.sina.com.cn/orignal/515359c4g79a1c1001942&690查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
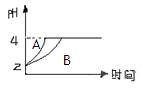
| A.反应开始时产生氢气的速率:盐酸 = 醋酸 |
| B.反应全过程产生氢气的平均速率:盐酸<醋酸 |
| C.反应停止后产生氢气的总量:盐酸<醋酸 |
| D.反应全过程溶解锌的质量:盐酸 = 醋酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
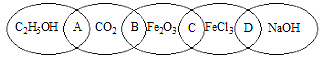
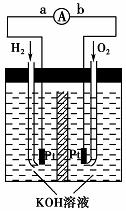
 该反应的化学方程式为_______
该反应的化学方程式为_______ _______________________________________________。
_______________________________________________。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.虽然固体氯化钠不能导电,但氯化钠是电解质 |
| B.纯水的pH随温度的升高而减小 |
| C.在醋酸钠溶液中加入少量氢氧化钠,溶液中c(OH—)增大 |
| D.在纯水中加入少量硫酸铵,可抑制水的电离 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.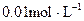 甲酸溶液 甲酸溶液 |
B.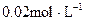 甲酸溶液与 甲酸溶液与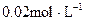 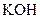 溶液等体积混合后所得的溶液 溶液等体积混合后所得的溶液 |
C.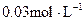 甲酸溶液与 甲酸溶液与 的 的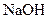 溶液等体积混合后所得的溶液 溶液等体积混合后所得的溶液 |
D.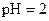 的硫酸与 的硫酸与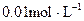 的 的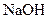 溶液等体积混合后所得的溶液 溶液等体积混合后所得的溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com