
 A、B、C、D、E、F 六种有机物.A能够在光照条件下与氯气发生取代反应,其二氯取代物有两种; B与溴的四氯化碳溶液可以发生加成反应,加成产物是D,且D只有一种同分异构体E;C在FeBr3 的作用下,可以与液溴发生取代反应,取代产物是F,F没有含苯环的同分异构体.根据以上事实,回答下列问题:
A、B、C、D、E、F 六种有机物.A能够在光照条件下与氯气发生取代反应,其二氯取代物有两种; B与溴的四氯化碳溶液可以发生加成反应,加成产物是D,且D只有一种同分异构体E;C在FeBr3 的作用下,可以与液溴发生取代反应,取代产物是F,F没有含苯环的同分异构体.根据以上事实,回答下列问题: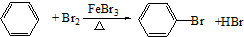 ;
;分析 A、B、C、D、E、F 六种有机物,A能够在光照条件下与氯气发生取代反应,其二氯取代物有两种,则A为CH3CH3,为CH3CHCl2或CH2ClCH2Cl;B与溴的四氯化碳溶液可以发生加成反应,加成产物是D,且D只有一种同分异构体E,则B为CH2=CH2,D为CH2BrCH2Br,E为CH3CHBr2,C在FeBr3 的作用下,可以与液溴发生取代反应,取代产物是F,F没有同分异构体,故C为苯( ),F为溴苯(
),F为溴苯( ),以此解答该题.
),以此解答该题.
解答 解:(1)A能够在光照条件下与氯气发生取代反应,其二氯取代物有两种,则A为CH3CH3,A的两种二氯取代物为:CH3CHCl2或CH2ClCH2Cl,
乙烷生成一氯取代物,乙烷分子中的一个氢原子被氯原子取代,方程式为:CH3CH3+Cl2$\stackrel{光照}{→}$CH3 CH2Cl+HCl,
故答案为:CH3CH3+Cl2$\stackrel{光照}{→}$CH3 CH2Cl+HCl;
(2)B与溴的四氯化碳溶液可以发生加成反应,加成产物是D,且D只有一种同分异构体E,反应为:CH2=CH2+Br2→CH2BrCH2Br,则B为CH2=CH2,D为CH2BrCH2Br,E为CH3CHBr2,D在氢氧化钠溶液中,为二溴乙烷的水解生成醇的反应,反应方程式为:CH2BrCH2Br+2H2O$→_{△}^{NaOH}$CH2OHCH2OH+2 HBr或CH2BrCH2Br+2 NaOH$→_{△}^{H_{2}O}$CH2OHCH2OH+2 NaBr,
故答案为:CH2BrCH2Br+2H2O$→_{△}^{NaOH}$CH2OHCH2OH+2 HBr或CH2BrCH2Br+2 NaOH$→_{△}^{H_{2}O}$CH2OHCH2OH+2 NaBr;
(3)B为CH2=CH2,B与溴的四氯化碳溶液发生加成反应CH2=CH2+Br2→CH2BrCH2Br,D为CH2BrCH2Br,E的同分异构体为D,所以E为CH3CHBr2,
故答案为:CH3CHBr2;
(4)C为苯( ),F为溴苯(
),F为溴苯( ),C生成F为苯与液溴在溴化铁的催化作用下生成溴苯,苯环上的一个氢原子被一个溴原子取代,其反应方程式为:
),C生成F为苯与液溴在溴化铁的催化作用下生成溴苯,苯环上的一个氢原子被一个溴原子取代,其反应方程式为: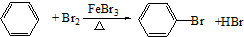 ,
,
故答案为: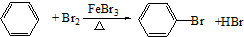 ;
;
(5)发生反应时可能会有苯、溴等挥发出来,苯呈中性,但液溴溶于水后,与水反应生成氢溴酸和次溴酸,所以将生成的气体通入右图所示的实验装置,通过四氯化碳溶液洗气,将溴蒸汽除去后,通过加入紫色石蕊试液或AgNO3溶液的乙装置,若出现溶液变红(或加入硝酸酸化的硝酸银溶液,出现淡黄色沉淀),有溴化氢生成,说明反应为取代反应,
故答案为:加入紫色石蕊试液;溶液变红(或加入硝酸酸化的硝酸银溶液,出现淡黄色沉淀).
点评 本题考查有机物的推断,是高考中的常见题型,题目难度中等,掌握苯的性质以及推断A为CH3CH3为解答该题的关键,侧重对学生能力的培养,旨在培养学生分析、归纳、总结问题的能力,有利于培养学生的逻辑推理能力和创新思维能力,此类题注意把握题给信息.


 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案科目:高中化学 来源: 题型:选择题
| A. | 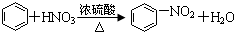 | |
| B. | 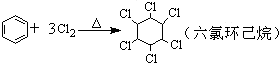 | |
| C. | 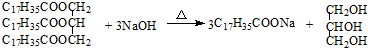 | |
| D. | CH3CH=CH2+Cl2$→_{△}^{500℃}$ClCH2CH═CH2+HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 物质A~G均由短周期元素组成,A、B为非金属气体单质,B原子最外层电子数比次外层电子数的2倍还多1.甲、乙均为金属单质,且甲的原子半径在第三周期最大.各物质间的转化关系如下(部分生成物未给出,且未注明反应条件):
物质A~G均由短周期元素组成,A、B为非金属气体单质,B原子最外层电子数比次外层电子数的2倍还多1.甲、乙均为金属单质,且甲的原子半径在第三周期最大.各物质间的转化关系如下(部分生成物未给出,且未注明反应条件):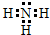 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | F2>Cl2>Br2>I2 | B. | CF4>CCl4>CBr4>CI4 | ||
| C. | HF<HCl<HBr<HI | D. | CH4<SiH4<GeH4<SnH4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3Cl2+6NaOH=2NaClO3+5NaCl+3H2O | |
| B. | CaH2+2H2O=Ca(OH)2+2H2↑ | |
| C. | AlCl3+3NaAlO2+6H2O=4Al(OH)3↓+3NaCl | |
| D. | 2CuO+Cu2S=4Cu+SO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
 向甲、乙两个容积均为1L的恒容容器中,分别充入2mol A、2mol B和1mol A、1mol B.相同温度下,发生反应:A(g)+B(g)?xC(g);△H<0.测得两容器中c(A)随时间t的变化如图所示.下列说法正确的是( )
向甲、乙两个容积均为1L的恒容容器中,分别充入2mol A、2mol B和1mol A、1mol B.相同温度下,发生反应:A(g)+B(g)?xC(g);△H<0.测得两容器中c(A)随时间t的变化如图所示.下列说法正确的是( )| A. | 甲、乙两容器中反应达平衡时,平衡常数K(甲)<K(乙) | |
| B. | x不可能等于2 | |
| C. | 将乙容器升温可使甲、乙容器内各物质的体积分数相同 | |
| D. | 若向甲容器中再充入2mol A、2mol B,则平衡时甲容器中0.78mol•L-1<c(A)<1.56mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素编号 | 元素性质或原子结构 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| T | 最外层电子数是电子层数的2倍 |
| Z | 元素最高正价是+7价 |
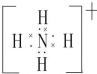 (用元素符号表示).
(用元素符号表示).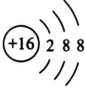 ,
,查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol•L-1硫化钠溶液中离子浓度关系:c(Na+)=2[c(S2-)+c(HS-)+c(H2S)] | |
| B. | 常温下醋酸分子不可能存在于pH>7的碱性溶液中 | |
| C. | 常温下向氯化铵溶液中加入少量氨水使溶液的pH=7,则混合溶液中:c(Cl-)>c(NH4+) | |
| D. | 0.1mol•L-1的氯化铵溶液与0.05mol•L-1的氢氧化钠溶液等体积混合后,混合溶液中离子浓度:c(Cl-)>c(NH4+)>c(Na+)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在饱和硫酸铜溶液中放入胆矾晶体,几天后晶体外形发生改变且晶体质量变小 | |
| B. | 将两块未擦去氧化膜的铝片分别投入1mol?L-1CuSO4溶液和1mol?L-1CuCl2溶液中,铝片表面都观察不到明显的反应现象 | |
| C. | 可用紫外可见分光光度法来测定溶液中苯酚的含量 | |
| D. | 在比较乙醇和苯酚与钠反应的实验中,要把乙醇和苯酚配成同物质的量浓度的水溶液,再与相同大小的金属钠反应,来判断两者羟基上氢的活性大小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com