
已知:25℃,Ksp[M(OH)2]=3.2×10﹣11,则此温度下M(OH)2饱和溶液的pH 等于()
A. 10 B. 10+lg2 C. 10+2×lg2 D. 10﹣2×lg2
科目:高中化学 来源: 题型:
下列各物质所含原子数目,按由大到小顺序排列的是( )
①0.5mol NH3 ②标准状况下22.4L氦气 ③4℃9mL水 ④0.2mol H3PO4.
|
| A. | ①④③② | B. | ④③②① | C. | ②③④① | D. | ①④②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
现有CO、CO2、O3(臭氧)三种气体,它们分别都含有1mol氧原子,则三种气体的物质的量之比为( )
|
| A. | 1:1:1 | B. | 1:2:3 | C. | 3:2:1 | D. | 6:3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
将2mol SO2和2mol SO3气体,充入固定体积的密闭容器,在一定条件下发生下列反应:2SO2+O2⇌2SO3,平衡时SO3为n mol,相同温度下,分别按下列配比在相同体积的密闭容器中加入起始物质,到达平衡时SO3的物质的量一定大于n mol的是()
A. 2mol SO2+1mol O2
B. 4mol SO2+1mol O2
C. 2mol SO2+1mol O2+2mol SO3
D. 3mol SO2+1mol SO3
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,0.2mol/L的一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是()
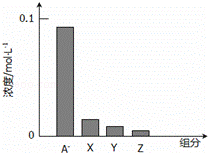
A. HA为强酸
B. 该混合液pH=7
C. 图中X表示HA,Y表示OH﹣,Z表示H+
D. 该混合溶液中:c(A﹣)+c(Y)=c(Na+)
查看答案和解析>>
科目:高中化学 来源: 题型:
钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的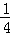 .
.
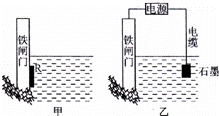
(1)为了降低某水库的铁闸门被腐蚀的速率,可以采用如图所示甲的方案,属于 原理(填“原电池”或“电解池”)
(2)图中乙方案也可降低铁闸门腐蚀速率,称为 保护法.
(3)将5mol/L CuSO4溶液200mL用惰性电极电解一段时间后,从其中的一个电极收集到标准状况下448mL气体,为使电解后的溶液恢复到开始的浓度,应向电解后的溶液中加入 物质(填化学式).
查看答案和解析>>
科目:高中化学 来源: 题型:
已知短周期元素形成的离子aA+、bB2+、cC﹣、dD2﹣均具有相同的电子层结构,下列判断正确的是( )
|
| A. | 元素的金属性:B>A;元素的非金属性:D>C |
|
| B. | 原子序数:b>a>c>d |
|
| C. | 离子半径:D2﹣>C﹣>B2+>A+ |
|
| D. | 原子半径:A>B>C>D |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列事实均能说明醋酸是弱电解质的是()
①醋酸与水能以任意比互溶
②醋酸溶液能导电
③醋酸溶液中存在醋酸分子
④0.1mol/L醋酸溶液的pH比0.1mol/L盐酸的pH大
⑤醋酸能和碳酸钙反应放出CO2
⑥大小相同的锌粒与相同物质的量浓度的盐酸和醋酸溶液反应,开始醋酸产生H2速率慢.
A. ②③⑥ B. ④⑤⑥ C. ③④⑥ D. ①②③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com