
X、Y、M、Z、R为前四周期元素,且原子序数依次增大。XY2是红棕色气体;X与氢元素可形成XH3;M是周期表中电负性最大的元素;Z基态原子的M层是K层电子数的3倍;R2+离子的3d轨道中有9个电子。请回答下列问题:
(1)基态Y原子的价电子排布图是______;Z所在周期中第一电离能最大的主族元素是_______(元素名称)
(2)XY2? 离子的立体构型是________;R2+的水合离子[R(H2O)4]2+中,提供孤电子对的原子是________(元素符号)。
(3) 已知XH3易与R2+形成配离子,但XM3不易与R2+形成配离子,其原因是_______________
(4)Y与R所形成的化合物晶体晶胞如右图所示,该晶体的化学式:_____________;晶胞参数如图所示,则该晶胞密度是_______________g·cm-3(列式并计算结果,保留小数点儿后一位)。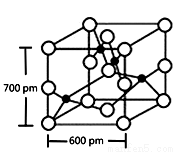
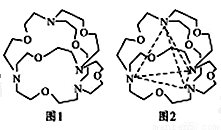
(5)图1表示某种含氮有机化合物的结构,其分子内4个氮原子分别位于正四面体的4个顶点(见图2),分子内存在空腔,能嵌入某离子或分子并形成4个氢键予以识别。下列分子或离子中,能被该有机化合物识别的是________(填标号)。
A.CF4 B.CH4 C.NH4+ D.H2O
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源:2015-2016学年广西桂林中学高二上期中考试理化学试卷(解析版) 题型:选择题
下列有关说法正确的是
A.聚氯乙烯的单体是CH3CH2Cl
B.乙醇和乙二醇为同系物
C.环己烷和丙烯的实验式相同
D.正戊烷、异戊烷、新戊烷的沸点逐渐升高
查看答案和解析>>
科目:高中化学 来源:2016届浙江临海台州中学高三上学期第三次统练化学试卷(解析版) 题型:选择题
氨基钠和氢化钠与水反应的化学方程式如下:①NaNH2+H2O=NaOH+NH3↑
②NaH+H2O==NaOH+H2↑,下列叙述正确的是
A.氨基钠和氢化钠与盐酸反应都只生成一种盐
B.方程式②中,每生成1mol H2转移1 mol电子
C.氨基钠和氢化钠的晶体中都只含离子键
D.方程式①中,氨基钠是还原剂
查看答案和解析>>
科目:高中化学 来源:2016届山西平遥中学等重点中学高三第三次练兵化学试卷(解析版) 题型:选择题
稀土金属铈(Ce)在空气中易氧化变暗,受热时燃烧,遇水很快反应。已知:①铈常见的化合价为+3和+4价;②氧化性:Ce4+> Ce3+。下列说法正确的是
A.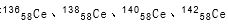 它们互称同素异形体
它们互称同素异形体
B.铈溶于氢碘酸的主要化学方程式可表示为2Ce+6HI=2CeI3+3H2↑
C.工业上可以采用电解氯化铈水溶液来获得铈单质
D.工业上金属铈一般保持在敞口容器中
查看答案和解析>>
科目:高中化学 来源:2016届宁夏回族自治区银川一中高三上第五次月考理化学试卷(解析版) 题型:填空题
硫代硫酸钠(Na2S2O3)在工业生产、医药制造业中被广泛应用,工业普遍使用Na2SO3与硫磺(S)共煮得到,装置如图1。
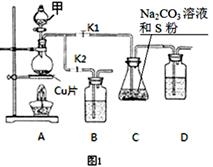
已知:Na2S2O3在酸性溶液中不能稳定存在。
(1)步骤1:打开K1、关闭K2,向圆底烧瓶中加入足量甲并加热,写出反应的方程式: 。
(2)步骤2:始终保持C中溶液呈碱性,反应一段时间后,硫粉的量逐渐减少,打开K2、关闭K1并停止加热。
①C中溶液须保持呈碱性的原因:若呈酸性,则 、 。(用离子方程式表示)
②装置B、D的试剂相同,均为 。
步骤3:将C中所得混合物分离提纯后得产品。
(3)利用反应2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2也能制备Na2S2O3。所需仪器如图2,按气流方向连接各仪器,接口顺序为:a→____,____→ , → , →d。
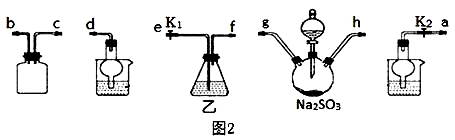
(4)装置乙盛装的试剂是:_____________________________。
(5)Na2S2O3还原性较强,工业上常用作除去溶液中残留的Cl2,该反应的离子方程式为 。
(6)请设计简单的实验方案,证明上述残留的Cl2被还原成了Cl—:____________
查看答案和解析>>
科目:高中化学 来源:2016届宁夏回族自治区银川一中高三上第四次月考理化学试卷(解析版) 题型:选择题
下列物质中均含有酸性杂质,除去这些杂质的方法中正确的是
A.乙醇中含乙酸杂质:加入足量氧化钙,蒸馏
B.制氯气时,依次通过饱和NaHCO3溶液和浓硫酸净化气体
C.CO2中混有H2S通过足量的浓硫酸溶液洗气,以得到纯净的CO2
D.通过灼热的镁粉除去N2中的O2
查看答案和解析>>
科目:高中化学 来源:2016届河北正定中学高三上学期第五次月考理科综合化学试卷(解析版) 题型:选择题
下列对定量实验误差分析正确的是
A.中和热测定实验中,缓慢地将NaOH溶液倒入测定装置中——测定结果无影响
B.酸碱中和滴定实验中,滴定前无气泡而滴定后有气泡——测定结果偏高
C.测定溶液pH的实验中,用干燥pH试纸测定新制氯水的pH——测定结果无影响
D.现需90 mL 1.0 mol/L NaOH溶液,称取3.6 g NaOH 固体配制——溶液浓度偏低
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南二校高一理科实验班上联考2化学卷(解析版) 题型:计算题
准确称取22.7g某矿石样品(含Al2O3、Fe2O3和不溶于水和酸的杂质),放入盛有100mL某浓度的硫酸的烧杯中,充分反应后过滤,向滤液中加入10mol/L的NaOH溶液,产生的沉淀的质量m与加入NaOH溶液的体积V的关系如下图所示。请回答:
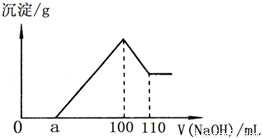
(1)硫酸的物质的量浓度是多少?
(2)若a=10,矿石样品中Fe2O3的质量是多少?
(3)试计算a的取值范围。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州省高二上二次月考化学试卷(解析版) 题型:选择题
已知1 g H2完全燃烧生成水蒸气时放出的热量121 kJ,且氧气中1 mol O=O键完全断裂时吸收热量496 kJ,水蒸气中1 molH-O键形成时放出热量463 kJ,则1 molH-H键断裂时吸收热量为
A.920 kJ B.557 kJ C.436 kJ D.188 kJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com