
【题目】下列说法正确的是
A. 按系统命名法,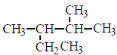 的名称为2-甲基-3-乙基丁烷
的名称为2-甲基-3-乙基丁烷
B. 聚乙烯(PE)和聚氯乙烯(PVC)的单体都是不饱和烃,均能使溴水褪色
C. 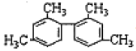 分子中至少有11个碳原子处于同一平面
分子中至少有11个碳原子处于同一平面
D. 有机物 与NaOH溶液反应,最多消耗4mol NaOH
与NaOH溶液反应,最多消耗4mol NaOH
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案科目:高中化学 来源: 题型:
【题目】位于短周期的四种主族元素A、B、C、D,原子序数依次增大,已知A、C位于同一主族,A在周期表中原子半径最小。B、D的最外层电子数相等,且B、D的原子序数之和为A、C原子序数之和的两倍。E是我国使用最早合金中的主要成分。根据你的推断完成下列问题:
(1)B、C、E的元素符号为________,________,__________。
(2)写出由上述元素形成的具有漂白作用的四种物质的化学式______、______、______、______。
(3)由A、B两种元素形成的原子个数比为1∶1的化合物的电子式______。
(4)写出D的最高价氧化物对应水化物与E反应的化学方程式,并用双线桥标出电子转移的方向和数目___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过海水晾晒可得粗盐,粗盐除NaCl外,还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质。以下是制备精盐的实验方案,各步操作流程如图:
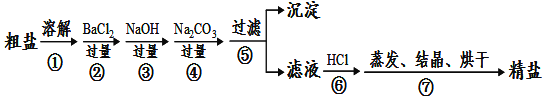
(1)在第①步粗盐溶解操作中要用玻璃棒搅拌,作用是______。
(2)第②步操作的目的是除去粗盐中的______(填化学式,下同),第⑥步操作的目的是除去滤液中______。
(3)第⑤步“过滤”操作中得到沉淀的成分有:泥沙、BaSO4、Mg(OH)2、______(填化学式)。
(4)在第③步操作中,选择的除杂的试剂不能用KOH代替NaOH,理由是______。
(5)实验所得精盐的质量大于粗盐中NaCl的质量,原因是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在标准状况下,22 g CO2的体积是________L,与________ g N2含有相同的分子数。
(2)等物质的量的CO和CO2其质量之比是________,分子数之比是________。
(3)同温同压下,同体积的氨气和硫化氢(H2S)气体的质量比为________;同质量的氨气和硫化氢气体体积比为________,其中含有的氢原子数目比为________;若二者氢原子数相等,则它们的体积比为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是一种实验某气体化学性质的实验装置,图中B为开关。如先打开B,在A处通入干燥的氯气,C中红色布条颜色无变化;当关闭B时,C处红色布条褪色。则D瓶中盛有的溶液是( )

A. 浓硫酸B. 饱和氯化钠溶液C. 浓氢氧化钠溶液D. 氢氧化钙悬浊液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《Journal of Energy Chemistry》报导我国科学家设计CO2熔盐捕获与转化装置如图。下列有关说法正确的是
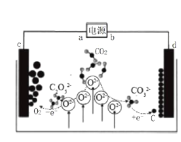
A. b为电源的正极
B. 电子流向:c→a→b→d
C. c极电极反应式为2C2O52――4e-=4CO2+O2
D. 转移0.4mol电子可捕获CO2 2.24L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某有机物X的结构简式如图所示,下列有关叙述不正确的是( )

A.X的化学式为C10H10O6
B.X在一定条件下能与FeCl3溶液发生显色反应
C.1 mol X分别与足量的Na、NaOH溶液、NaHCO3溶液反应,消耗这三种物质的物质的量分别为3 mol、4 mol、1 mol
D.X在一定条件下能发生消去反应和酯化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以黄铜矿(CuFeS2)、FeCl3和乳酸[CH3CH(OH)COOH]为原料可制备有机合成催化剂CuCl和补铁剂乳酸亚铁{[CH3CH(OH)COO]2Fe}。其主要实验流程如下:
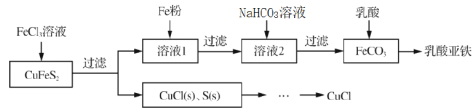
已知:①乳酸亚铁是绿白色晶体,溶于水,几乎不溶于乙醇。
②CuCl为白色晶体,难溶于水和乙醇,在空气中易氧化;可与NaCl溶液反应,生成易溶于水的NaCuCl2。
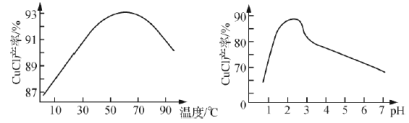
③NaCuCl2可水解生成CuCl,温度、pH对CuCl产率的影响如图所示。
(1)FeCl3溶液与黄铜矿发生反应的离子方程式为_______________。
(2)向溶液1中加入过量铁粉的目的是______________。
(3)下列有关实验说法不正确的是______________。(填编号)
A.减压过滤使用的滤纸,为确保把所有的孔都覆盖住,应使滤纸大于布氏漏斗内径
B.为得到干燥的乳酸亚铁晶体,采用高温烘干的方式干燥
C.洗涤CuCl沉淀时,关小抽气泵,向布氏漏斗中加乙醇没过沉淀,并用玻璃棒搅拌
D.为得到较大的乳酸亚铁晶体颗粒,可投入几粒晶种并减缓溶液冷却速度
(4)若向NaHCO3溶液中加入FeSO4溶液,得到的FeCO3不纯,其原因是___________。
(5)用高锰酸钾标准液测定乳酸亚铁产品纯度,配制该标准溶液时,下列仪器中不必要用到的有_________。(用编号表示)。
①电子天平 ②烧杯 ③量筒 ④玻璃棒 ⑤容量瓶 ⑥胶头滴管 ⑦移液管
下列操作会引起结果偏高的是____________(用编号表示)。
A.滴定前,滴定管和锥形瓶分别用标准液与待测液润洗
B.配制高锰酸钾溶液定容时,仰视刻度线
C.滴定前滴定管尖嘴内无气泡,滴定后尖嘴内有气泡
D.加待测液前锥形瓶内有少量水
E.滴定前俯视读数,滴定后仰视读数
(6)由CuCl(s)、S(s)混合物提纯CuCl的实验方案为:将一定量的混合物溶于饱和NaCl溶液中,_______。(需要用到下列所有操作,给出正确的顺序)
①滤液加热至60℃左右 ②趁热过滤 ③过滤 ④用乙醇洗净所得固体
⑤滴加加0.1mol·L-1H2SO4至pH为2.0~2.5 ⑥置于真空干燥箱中干燥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值,下列叙述错误的是( )
A. 1.8gH2O中含有的质子数为NA
B. 22.4L氯气与足量镁粉充分反应,转移的电子数为2NA
C. 46gNO2和N2O4混合气体中含有原子总数为3NA
D. 23gNa与足量O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com