
【题目】已知烃B分子内C、H原子个数比为1︰2,相对分子质量为28,核磁共振氢谱显示分子中只有一种化学环境的氢原子,且有如下的转化关系:
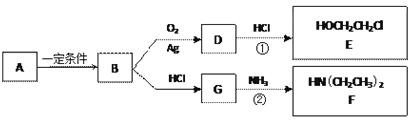
(1)B的结构简式是_________________
(2)A可能属于下列哪类物质___________
a.醇 b.卤代烃 c.酚 d.羧酸
(3)反应①是D与HCl按物质的量之比1︰1的加成反应,则D的分子式是___________。
反应②可表示为:G + NH3→ F + HCl (未配平),该反应配平后的化学方程式是(有机化合物均用结构简式表示): ____________________________________
化合物E(HOCH2CH2Cl)和 F [ HN(CH2CH3)2 ]是药品普鲁卡因合成的重要中间体,普鲁卡因的合成路线如下:(已知:![]() )
)

(4)甲的结构简式是 _________________。
由甲苯生成甲的反应类型是_________________。
(5)乙中有两种含氧官能团,反应③的化学方程式是___________________________________
(6)丙中官能团的名称是_______________________________________。
(7)普鲁卡因有两种水解产物丁和戊。
① 戊与甲互为同分异构体,戊的结构简式是_____________________。
② 戊经聚合反应制成的高分子纤维广泛用于通讯、宇航等领域。该聚合反应的化学方程式是__________________________________________。
③ D的红外光谱表明分子内除C—H键、C—C键外还含有两个C—O单键。则D与F在一定条件下反应生成丁的化学方程式是________________________________。
【答案】CH2=CH2 ab C2H4O 2CH3CH2Cl + NH3→NH(CH2CH3)2 +2HCl ![]() 取代反应(或硝化反应)
取代反应(或硝化反应) ![]() +HOCH2CH2Cl
+HOCH2CH2Cl![]()
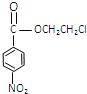 +H2O 酯基、氯原子、氨基
+H2O 酯基、氯原子、氨基 ![]()
![]()
![]()
【解析】
烃B分子内C、H原子个数比为1:2,相对分子质量为28,令B的分子式为CnH2n,则14n=28,解得n=2,核磁共振氢谱显示分子中只有一种化学环境的氢原子,则B为CH2=CH2,A可能为卤代烃或醇,发生消去反应生成乙烯,B→D发生氧化反应,反应①是D与HCl按物质的量之比1:1的加成反应,E的结构简式为HOCH2CH2Cl,D的分子式为C2H4O;B与HCl发生加成反应生成G,G为CH3CH2Cl,G与氨气发生取代反应生成F,据此解答。
由普鲁卡因的合成路线可以知道,甲苯发生硝化反应生成的甲为![]() ,甲发生氧化反应生成的乙为
,甲发生氧化反应生成的乙为![]() ,乙与E发生酯化反应生成
,乙与E发生酯化反应生成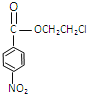 ,
,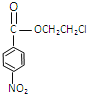 中硝基被还原为氨基生成的丙为
中硝基被还原为氨基生成的丙为 ,丙与F发生取代反应生成普鲁卡因,然后结合物质的性质来解答。
,丙与F发生取代反应生成普鲁卡因,然后结合物质的性质来解答。
烃B分子内C、H原子个数比为1:2,相对分子质量为28,令B的分子式为CnH2n,则14n=28,解得n=2,核磁共振氢谱显示分子中只有一种化学环境的氢原子,则B为CH2=CH2,A可能为卤代烃或醇,发生消去反应生成乙烯,B→D发生氧化反应,反应①是D与HCl按物质的量之比1:1的加成反应,E的结构简式为HOCH2CH2Cl,D的分子式为C2H4O;B与HCl发生加成反应生成G,G为CH3CH2Cl,G与氨气发生取代反应生成F;
由普鲁卡因的合成路线可以知道,甲苯发生硝化反应生成的甲为![]() ,甲发生氧化反应生成的乙为
,甲发生氧化反应生成的乙为![]() ,乙与E发生酯化反应生成
,乙与E发生酯化反应生成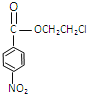 ,
,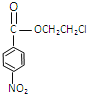 中硝基被还原为氨基生成的丙为
中硝基被还原为氨基生成的丙为 ,丙与F发生发生取代反应生成普鲁卡因;
,丙与F发生发生取代反应生成普鲁卡因;
(1)由上述分析可以知道,B的结构简式为CH2=CH2;
(2
(3)反应①是D与HCl按物质的量之比1:1的加成反应,E的结构简式为HOCH2CH2Cl,则D的分子式为C2H4O ;反应②为2CH3CH2Cl+NH3→NH(CH2CH3)2+2HCl;
(4)由上述分析可以知道,甲为对硝基甲苯,结构简式为![]() ;由甲苯生成甲的反应类型是取代反应(或硝化反应);
;由甲苯生成甲的反应类型是取代反应(或硝化反应);
(5)乙为![]() ,含有的官能团为羧基、硝基,反应③的反应方程式为:
,含有的官能团为羧基、硝基,反应③的反应方程式为:![]() +HOCH2CH2Cl
+HOCH2CH2Cl![]()
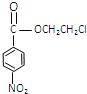 +H2O;
+H2O;
(6)丙为 ,其中含有官能团的名称是酯基、氯原子、氨基;
,其中含有官能团的名称是酯基、氯原子、氨基;
(7)①普鲁卡因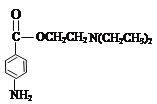 的水解产物有两种,分别是:
的水解产物有两种,分别是:![]() 、HOCH2CH2N(CH2CH3)2,其中
、HOCH2CH2N(CH2CH3)2,其中![]() 和
和![]() 互为同分异构体,则戊的结构简式为
互为同分异构体,则戊的结构简式为![]() ;
;
②![]() 中氨基和羧基发生缩聚反应,生成
中氨基和羧基发生缩聚反应,生成 ,该聚合反应的化学方程式是
,该聚合反应的化学方程式是 ![]() ;
;
③D的分子式为C2H4O,D的红外光谱表明分子内除C—H键、C—C键外还含有两个C—O单键,D的结构简式为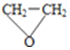 ,D与F在一定条件下反应生成丁[HOCH2CH2N(CH2CH3)2]的化学方程式是
,D与F在一定条件下反应生成丁[HOCH2CH2N(CH2CH3)2]的化学方程式是![]() 。
。


科目:高中化学 来源: 题型:
【题目】丁苯酞(J)是治疗轻、中度急性脑缺血的药物,合成J的一种路线如下:
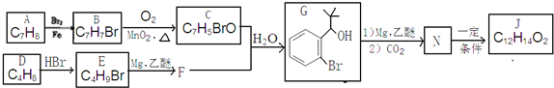
已知:①R-Br![]()
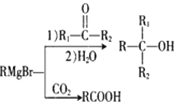
②E的核磁共振氢谱只有一组峰;
③C能发生银镜反应;
④J是一种酯,分子中除苯环外还含有一个五元环。
回答下列问题:
(1)由A生成B的化学方程式为__________,其反应类型为__________;
(2)D的化学名称是__________,由D生成E的化学方程式为__________;
(3)J的结构简式为__________;
(4)G的同分异构体中核磁共振氢谱有4组峰且能与FeCl3溶液发生显色反应的结构简式__________(写出一种即可);
(5)由甲醛和化合物A经下列步骤可得到2—苯基乙醇:A![]() K
K![]() L
L![]()
![]() 。反应条件1为__________;反应条件2所选择的试剂为__________;L的结构简式为__________。
。反应条件1为__________;反应条件2所选择的试剂为__________;L的结构简式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向100mL0.01mol·L-1HA溶液中逐滴加入0.02mol·L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。回答下列问题:
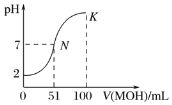
(1)由图中信息可知HA为________(填“强”或“弱”)酸,MOH为_________(填“强”或“弱”)碱。
(2)常温下一定浓度的MA稀溶液的pH=a,则a______(填“>”“<”或“=”)7,用离子方程式表示其原因:__________________,此时溶液中由水电离出的c(OH-)=____________。
(3)K点对应的溶液中,c(M+)+c(MOH)________(填“>”“<”或“=”)2c(A-),溶液中离子浓度的大小关系:__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钛(Ti)是一种具有许多优良性能的金属,钛和钛合金被认为是21世纪的重要金属材料。
(1)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。
①Ti2+基态电子排布式可表示为_____。
②与BH4-互为等电子体的阳离子的化学式为_____。
③H、B、Ti原子的第一电离能由小到大的顺序为_____。
(2)二氧化钛(TiO2)是常用的、具有较高催化活性和稳定性的光催化剂,常用于污水处理。纳米TiO2催化的一个实例如图所示。
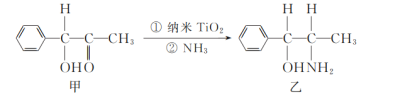
化合物乙的分子中采取sp3杂化方式的原子个数为_____。
(3)水溶液中并没有[Ti(H2O)6)]4+离子,而是[Ti(OH)2(H2O)4]2+离子,1mol[Ti(OH)2(H2O)4]2+中σ键的数目为____。
(4)氮化钛(TiN)具有典型的NaCl型结构,某碳氮化钛化合物,结构是用碳原子取代氮化钛晶胞(结构如图)顶点的氮原子,则此碳氮化钛化合物的化学式是_____。
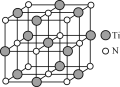
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】玻璃钢可由酚醛树脂和玻璃纤维制成。
(1)酚醛树脂由酚醛和甲醛缩聚而成,反应有大量热放出,为防止温度过高,应向有苯酚的反应釜___________加入甲醛,且反应釜应装有________________装置。
(2)玻璃纤维由玻璃拉丝得到。普通玻璃由石英砂、___________和石灰石(或长石)高温熔融而成,主要反应的化学方程式为______________。
(3)玻璃钢中玻璃纤维的作用是____________。玻璃钢具有__________等优异性能(写出两点即可)
(4)下列处理废旧热固性酚醛塑料的做法合理的是_____________
a.深埋
b.粉碎后用作树脂填料
c.用作燃料
d.用有机溶剂将其溶解,回收树脂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】莽草酸是一种合成治疗禽流感药物达菲的原料,鞣酸存在于苹果、生石榴等植物中。下列关于这两种有机化合物的说法正确的是( )
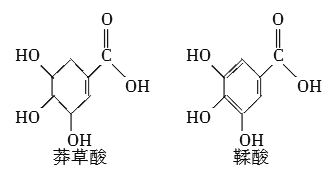
A.两种酸都能与溴水发生加成反应
B.两种酸与三氯化铁溶液都能发生显色反应
C.鞣酸分子与莽草酸分子相比多了两个碳碳双键
D.等物质的量的两种酸与足量的金属钠反应产生氢气的量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2﹣羟基异丁酸乙酯能溶于水,是一种应用于有机合成和药物制造的化工原料。

(1)2﹣羟基异丁酸乙酯的分子式为_________,不同化学环境的氢在核磁共振氢谱图中有不同的吸收峰,则2﹣羟基异丁酸乙酯有_________个吸收峰;
(2)①②的反应类型分别为_________,_________;
(3)已知I为溴代烃,I→B的化学方程式为_________;
(4)缩聚产物F的结构简式为_________;
(5)下列关于![]() 和
和 的说法正确的有_________(双选,填字母);
的说法正确的有_________(双选,填字母);
A.后者遇到FeCl3溶液显紫色,而前者不可
B.两者都可以与NaHCO3溶液反应放出CO2
C.两者都可以与氢氧化钠溶液发生反应,当两者物质的量相等时,消耗氢氧化钠的量不相等
D.两者都可以与氢气发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼、硅、硒等元素及其化合物用途广泛。请回答下列问题:
(1)基态硒原子的价电子排布式为_______;SeO2常温下为白色晶体,熔点为340~350℃,315℃时升华,则SeO2固体为________晶体。
(2)在硼、硅、硒的气态氢化物中,其立体构型为正四面体的是_______(填化学式),在硅的氢化物中共用电子对偏向氢元素,氢气与硒反应时单质硒是氧化剂,则硒与硅的电负性大小为Se_____Si(填“>”或“<”)。
(3)在周期表的第二周期中,第一电离能介于硼元素和氮元素之间的元素有_____种。
(4)硼元素具有缺电子性(价电子数少于价层轨道数),其化合物可与具有孤对电子的分子或离子生成配合物,如BF3能与NH3反应生成BF3·NH3,BF3·NH3中B与N之间形成______键;NH3中N原子的杂化轨道类型为______,写出与NH3等电子体的一种离子符号________。
(5)金刚砂(SiC)的摩氏硬度为9.5,其晶胞结构如图所示。在SiC中,每个Si原子周围距离最近的Si原子数目为________;若金刚砂的密度为ρg·cm-3,NA表示阿伏加德罗常数的值,则晶胞中碳原子与硅原子的最近距离为________pm。(用含ρ和NA的式子表示)
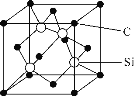
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应3A(g)![]() 3B+C ΔH>0,随着温度的升高,气体的平均相对分子质量有变小的趋势。下列关于B、C两种物质的聚集状态的判断不正确的是( )
3B+C ΔH>0,随着温度的升高,气体的平均相对分子质量有变小的趋势。下列关于B、C两种物质的聚集状态的判断不正确的是( )
A.B和C可能都是气体
B.B和C一定都是气体
C.若C为固体,则B一定是气体
D.有可能B为固体,C为气体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com