
(1)被氧化的Cu的物质的量为_________mol;
(2)被还原的HNO3的物质的量为_________mol;
(3)未被还原的硝酸的分子个数为_________;
(4)生成_________mol的NO;
(5)参加反应的硝酸的物质的量为_________mol。
科目:高中化学 来源: 题型:阅读理解
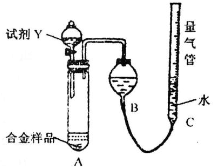
| 足量试剂X |
| 足量O2充分灼烧 |
| 密封(容器带自由移动的活塞) |
| ||
| 足量试剂Y |
| 1-V3 |
| 6.72 |
| 1-V3 |
| 6.72 |
查看答案和解析>>
科目:高中化学 来源:素质教育新教案 高中化学·二年级·第二册(上册) 题型:043
已知NH3和CuO反应可得较纯净的铜和氮气.现利用氨的还原性来测定氨分子中各元素的百分组成,同时也测定氨氧化的百分率.在反应中生成的气体用排水法测出其体积(假设水的体积为标准状况下气体的体积).
(1)下述装置连接成整套实验装置(填写各接口字母).
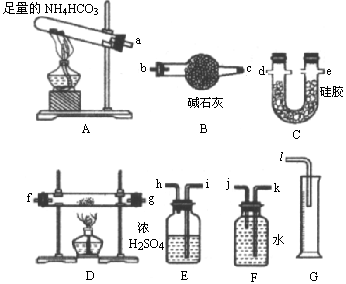
a接( )( )接( )( )接( )( )接( )( )接( )( )接( ).
(2)整套装置安装完毕后,检验气密性的方法是________.
(3)仪器连接好进行实验时,先点燃________处酒精灯,实验结束时应撤去________处酒精灯,且应________再熄灭________处的酒精灯,其理由是________.
(4)装置B的作用是________,装置C的作用是________,装置E的作用是________.
(5)写出D装置中发生反应的化学方程式________.
(6)测得D装置中试剂质量减少了m g,C装置中质量增加了n g,E装置中质量增加了x g,G装置中水的体积为y L,则NH3中氮原子数与氢原子数之比为(用m,n,y表示)________,被氧化NH3的质量百分含量为(用x,y表示)________.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 测定剩余固体质量.
测定剩余固体质量. 测定数据
测定数据 Mg3N2]
Mg3N2] 测定生成无色气体的体积
测定生成无色气体的体积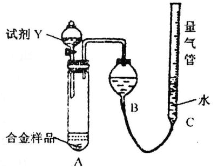
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com