
【题目】苯酚(结构简式如图所示),俗称石炭酸。是一种重要的化工原料,广泛用于制适酚醛树脂、染料、医药、农药等。下列说法不正确的是( )

A.分子中所有原子可能共平面
B.固体苯酚分子间可能形成氢键
C.![]() 该分子充分燃烧,会消耗
该分子充分燃烧,会消耗![]()
D.![]() 该分子与足量的氢气加成后,环上的一氯取代物有3种
该分子与足量的氢气加成后,环上的一氯取代物有3种
 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:
【题目】磷酸氯喹(结构如图所示)在细胞水平上能有效抑制新型冠状病毒的感染,我国印发的《新型冠状病毒肺炎诊疗方案(试行第七版)》中明确规定了其用量。
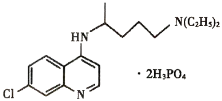
(1)碳、硅、锗为同一主族元素,则基态硅原子核外电子的空间运动状态有________种,基态锗原子的最外层的电子排布图为__________________。
(2)C、N、O三种元素第一电离能由大到小的顺序是_____________________。
(3)磷酸氯喹分子中氮原子的杂化方式为________,苯环中含有的共价键类型是________。
(4)![]() 的空间构型是____________,与
的空间构型是____________,与![]() 互为等电子体的分子是____________(写一种即可)。
互为等电子体的分子是____________(写一种即可)。
(5)由C、H、O元素组成的H2O和C2H5OH可以任意比例互溶,其原因是________________。
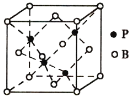
(6)由P与B元素形成的化合物BP的晶胞(如图所示)中B采用面心立方堆积,P原子填入四面体空隙中。已知晶胞边长为a pm,晶体中B原子与P原子的最近距离是___________,设阿伏加德罗常数的值为NA,则BP晶体的密度是___________g/cm3(列出计算表达式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业废气、汽车尾气排放出的SO2、NOx等,是形成雾霾的重要因素。霾是由空气中的灰尘、硫酸、硝酸、有机碳氢化合物等粒子形成的烟雾。
(1)NOx和SO2在空气中存在下列平衡:2NO(g)+O2(g)2NO2(g)△H=-113.0kJmol-1,2SO2(g)+O2(g)2SO3(g)△H=-196.6kJmol-1;SO2通常在二氧化氮的存在下,进一步被氧化,生成SO3。
①写出NO2和SO2反应的热化学方程式为__。
②随温度升高,该反应化学平衡常数变化趋势是___。
(2)提高2SO2+O22SO3反应中SO2的转化率,是减少SO2排放的有效措施。
①T温度时,在1L的密闭容器中加入2.0molSO2和1.0molO2,5min后反应达到平衡,二氧化硫的转化率为50%,该反应的平衡常数是__。
②在①中条件下,反应达到平衡后,改变下列条件,能使SO2的转化率提高的是___(填字母)。
a.温度和容器体积不变,充入1.0molHe b.温度和容器体积不变,充入1.0molO2
c.在其他条件不变时,减少容器的体积 d.在其他条件不变时,改用高效催化剂
e.在其他条件不变时,升高体系温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定条件下能大量共存的是( )
A.使甲基橙呈黄色的溶液中:Na+、Fe3+、Cl-、CO32-
B.使pH 试纸显蓝色的溶液中:K+、Na+、NO3-、SO42-
C.由水电离出的c(H+)=1×10-12mol·L-1的溶液中:Na+、Mg2+、Cl-、HCO3-
D. ![]() = 1×1012的溶液中:Fe3+、K+、CO32-、ClO-
= 1×1012的溶液中:Fe3+、K+、CO32-、ClO-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知非金属单质硫(S)是淡黄色固体粉末,难溶于水。为了验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题:

(1)装置A的分液漏斗中盛装的试剂是______,烧瓶中发生的反应的化学方程式是________。
(2)画出虚线框内的实验装置图,所加试剂为____________,该装置的作用是_______。
(3)装置B中盛放的试剂是____________(填序号),实验现象为____________,该反应的离子方程式是_____________,该反应属于四种基本反应类型中的__________反应。
A Na2S溶液 B Na2SO3溶液 C Na2SO4溶液
(4)已知:①硫酸比次氯酸稳定;②高氯酸的酸性比硫酸强;③S2-比Cl-易被氧化;④HCl比H2S稳定;⑤铜与盐酸不反应,但能与浓硫酸反应;⑥铁与氯气在加热条件下反应生成三氯化铁,铁与硫在加热条件下反应生成硫化亚铁;⑦硫原子与氯原子的电子层数相同,氯的原子半径小于硫原子。能说明氯的非金属性比硫强的是________(填序号)。
A 全部 B ②③④⑥⑦ C ①②④⑤⑥ D ②③④⑤⑥⑦
(5)装置C中盛放烧碱溶液,目地是吸收反应后剩余的气体,防止污染空气,写出该装置中所发生反应的离子方程式:_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了除去CuCl2酸性溶液中的FeCl3,加热搅拌的条件下加入一种试剂,然后再加入适量盐酸,该试剂不能是( )
A.Cu(OH)2B.CuCO3C.NaOHD.CuO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、回答下列问题:
(1)0.005mol/L 的H2SO4溶液的pH为_______。
(2)常温时,0.1mol/L的NaOH和0.06mol/L 的HCl溶液等体积混合,求混合溶液的pH为_______。
(3)某温度时,测得0.01 mol·L-1的NaOH溶液的pH为11,则该温度下水的离子积常数KW=___,该温度___ (填“高于”或“低于”)25 ℃。
(4)常温下,pH=13的Ba(OH)2溶液a L与pH=3的H2SO4溶液b L混合(混合后溶液体积变化忽略不计)。若所得混合溶液呈中性,则a∶b=________。
(5)氯化铁水溶液呈酸性,原因是(用离子方程式表示):___________。实验室在临时配制一些氯化铁溶液时,常将氯化铁固体先溶于较浓的_______中,然后再用蒸馏水稀释到所需的浓度,是为了抑制其水解。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱式硫酸铁[Fex(OH)y(SO4)z](其中Fe元素为+ 3价)是一种新型高效絮凝剂。一种利用废铁屑(含Fe和少量Al2O3、Fe2O3)生产碱式硫酸铁的工艺流程如下:
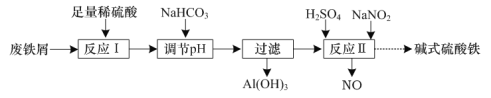
下列说法正确的是
A.x、y、z一定符合关系式:x=y=z
B.“过滤”所得滤液中只含溶质FeSO4
C.“反应Ⅰ”中包含的反应类型有置换反应、化合反应和复分解反应
D.在实际生产中,反应Ⅱ常同时通入O2以减少NaNO2的用量,若有11.2 L(标准状况)的O2参与反应,则相当于节约2 mol NaNO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某酸件废水可能含有Fe2+、Fe3+、Al3+、Mg2+、Na+、K+、CO32-、SO42-。取废水祥品分别进行如图所示①~④四个实验。下列推断正确的是
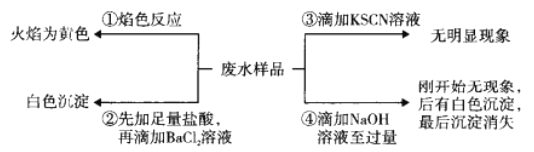
A. 废水含有Na+,不含K+
B. 废水含有SO42-和CO32-
C. 废水不含Fe3+,可能含Fe2+
D. 废水一定含有Na+、Al3+、SO42-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com