
| A. | 单位时间内消耗CO和CO2的物质的量相等时,反应达到平衡 | |
| B. | 使用高效催化剂可有效提高正反应速率 | |
| C. | 反应达到平衡后,NO的反应速率保持恒定 | |
| D. | 升高温度可使该反应的逆反应速率降低 |
分析 A、单位时间内消耗CO和CO2的物质的量相等时,即正、反应速率相等;
B、催化剂能够提高反应速率;
C、反应达到平衡状态时,正逆反应速率相等且保持不变;
D、升温正逆反应速率都加快.
解答 解:A、单位时间内消耗CO和CO2的物质的量相等时,即正、反应速率相等,反应达到平衡,故A正确;
B、催化剂能够加快反应速率,故B正确;
C、反应达到平衡后,正、逆反应速率相等且保持恒定,故C正确;
D、升温正逆反应速率都加快,故D错误;
故选D.
点评 本题考查了化学反应速率的影响因素和化学平衡状态的判断,注意选项D中涉及到反应平衡和反应速率问题,不管是吸热还是放热反应,当温度升高时候,反应速率都加快,温度降低,速率都降低,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 若X>Y,则酸性:HA>HB | |
| B. | 若X=Y,则HB一定是强酸 | |
| C. | 若酸性:HA<HB,则X和Y关系不确定 | |
| D. | 若由水电离出的H+的浓度:(I)>(Ⅱ),则是X>Y |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

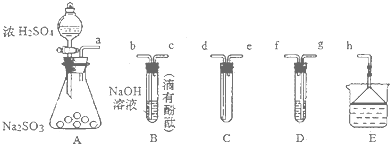
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 测定序号 | 待测溶液的体积/mL | 所耗盐酸标准液的体积/mL | |
| 滴定前 | 滴定后 | ||
| 1 | 20.00 | 0.50 | 20.52 |
| 2 | 20.00 | 1.20 | 21.18 |
| 3 | 20.00 | 0.80 | 24.20 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
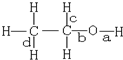
| A. | 和乙酸发生酯化反应键a断裂 | |
| B. | 和氢溴酸反应键a断裂 | |
| C. | 在铜催化和加热条件下和氧气反应键a、c断裂 | |
| D. | 和浓硫酸共热至170℃时键b和d断裂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 对空气进行降温加压 | B. | 金刚石变成石墨 | ||
| C. | NaCl熔化 | D. | 碘溶于CCl4中 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
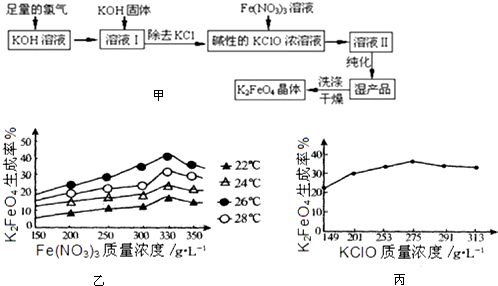
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A>C>D>B | B. | A>B>C>D | C. | C>A>D>B | D. | C>B>D>A |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com