
下列说法正确的是
A.向AgCl悬浊液中加入少量NaCl固体后振荡,c(Cl-)增大,KsP (AgCl)增大
B.某溶液中由水电离出的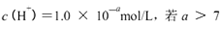 时,则该溶液的pH一定为14-a
时,则该溶液的pH一定为14-a
C. pH=3的二元弱酸H2R溶液与pH=11的NaOH溶液混合后溶液的pH等于7,则混合溶液
中: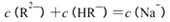
D.相同物质的量浓度的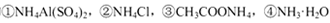 溶液中,c (NH4+)由大到小的顺序是:①>②>③>④
溶液中,c (NH4+)由大到小的顺序是:①>②>③>④
D
【解析】
试题分析:A、向AgCl悬浊液中加入少量NaCl固体后振荡,c(Cl-)增大,KsP (AgCl)不变,错误;B、如果该溶液为碱的溶液,水电离出的c(H+)=1.0×10-a mol?L?1,该溶液的pH为a,错误;C、根据电荷守恒可得:c(Na+)+c(H+)=c(OH?)+2c(R2-)+c(HR-),pH等于7,则c(H+)=c(OH?),所以c(Na+)= +2c(R2-)+c(HR-),错误;D、NH4Al(SO4)2 中NH4+与Al3+的水解相互抑制,CH3COONH4中CH3COO?与NH4+的水解相互促进,NH3?H2O为弱碱,电离出少量的NH4+,所以c (NH4+)由大到小的顺序是:①>②>③>④,正确。
考点:本题考查沉淀溶解平衡、盐类的水解、pH的计算、离子浓度比较。


 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源:2013-2014湖南师大附中第二学期期中考试高一化学试卷(解析版) 题型:选择题
化学反应一般均会伴随着能量变化,对H2在O2中燃烧的反应,正确的是
A.该反应为吸热反应 B.该反应为放热反应
C.断裂H-H键放出能量 D. 生成H-O键吸收能量
查看答案和解析>>
科目:高中化学 来源:2013-2014湖北省高三5月模拟考试理综化学试卷(解析版) 题型:选择题
下列事实、离子方程式及其对应关系均正确的是.
A.向淀粉碘化钾溶液中滴加稀硫酸,在空气中放置一段时间后溶液变蓝:4H++4I-+O2=2I2+2H2O
B.向K2Cr2O7溶液中滴加少量浓硫酸,溶液变为黄色: Cr2O72-(橙色)+H2O 2CrO42-(黄色)+2H+
2CrO42-(黄色)+2H+
C.0.01 mol·L-1NH4Al(SO4)2溶液与0.02 mol·L-1Ba(OH )2溶液等体积混合有白色沉淀生成:
Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O
D.用铜电极电解饱和食盐水:2Cl-+2H2O  Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
查看答案和解析>>
科目:高中化学 来源:2013-2014湖北省高一下学期期中联考化学试卷(解析版) 题型:选择题
应用元素周期表和元素周期律分析下列推断,其中正确的组合是
①根据元素周期律,由HClO4可类推出氟元素也存在HFO4
②在元素周期表的金属和非金属分界线附近寻找半导体材料
③铊(Tl)与铝同主族,原子核外有6个电子层,推测Tl(OH)3是两性氢氧化物
④碱金属单质和卤素单质的熔点都随原子序数的增大而增大
⑤砹(At)是VIIA族元素,其氢化物的稳定性大于HC1
⑥第三周期金属元素的最高价氧化物对应水化物,其碱性随原子序数的增大而减弱
A.②⑥ B.①③④ C.②③⑤ D.④⑥
查看答案和解析>>
科目:高中化学 来源:2013-2014湖北省武汉市高三四月调考理综化学试卷(解析版) 题型:简答题
(15分)
亚硝酸钠(NaNO2)易溶于水,微溶于乙醚,是常用的食品发色剂
(1)第一电离能:N ___O(填“<”、“>”或“=”);NO2-的空间构型为____
(2)亚硝酸钠在3200C会分解生成氧化钠、一氧化二氮等物质,该反应的化学方程式为____
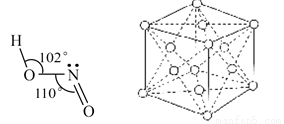
(3)亚硝酸钠是亚硝酸的钠盐。HNO2的结构如图所示,则HNO2分子中有___个 键:
键:
HNO2的酸性比HN03弱是因为_____
(4)亚硝基钻钠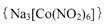 是钴的一种配合物,易溶于水,与钾离子反应生成淡黄色的
是钴的一种配合物,易溶于水,与钾离子反应生成淡黄色的
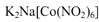 沉淀,可用于检验K+的存在。
沉淀,可用于检验K+的存在。
①基态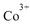 的价层电子排布图为_____
的价层电子排布图为_____
②用亚硝酸钻钠检验K+的离子方程式是
③金属钴的堆积方式如图所示,若一个钴原子的半径为r,,则晶胞的体积V(晶胞)=__
查看答案和解析>>
科目:高中化学 来源:2013-2014湖北省武汉市高三四月调考理综化学试卷(解析版) 题型:选择题
下列说法正确的是
A.用精密pH试纸测得饱和氯水的pH约为2.2
B.配制一定物质的量浓度的溶液,定容时仰视刻度,溶液浓度偏小
C.在中和滴定实验中,锥形瓶需用待测液润洗
D.制备乙酸乙酯时,将乙醇和乙酸依次加入浓硫酸中
查看答案和解析>>
科目:高中化学 来源:2013-2014湖北省武汉外国语学校高一下学期期中考试化学试卷(解析版) 题型:选择题
将15.6gNa2O2和5.4gAl同时放入一定量的水中,充分反应后得到200mL澄清溶液,再向该溶液中缓慢通入标准状况下的HCl气体6.72L,若反应过程中溶液的体积保持不变,则
A.反应过程中得到6.72L的气体(标准状况下)
B.最终得到的溶液中c(Na+)=c(Cl-)+c(OH-)
C.最终得到7.8g的沉淀
D.最终得到的溶液中c(NaCl)=1.6 mol/L
查看答案和解析>>
科目:高中化学 来源:2013-2014湖北省宜昌市高三5月模拟理综化学试卷(解析版) 题型:填空题
【化学–选修3:物质结构与性质】(15分)
X、Y、Z、W四种元素原子序数依次增大且均小于36。 Z基态原子最外层电子数是其内层电子总数的3倍,Y基态原子是同周期元素中未成对电子数最多的原子,X分别与Y、Z元素组合均可形成10电子微粒, W基态原子有10个价电子。回答下列问题(以下问题均以推知元素符号作答):
(1)若 YX3与X2Z﹑YX2-与ZX-﹑Y3-与Z2-性质相似,请写出Mg(YX2)2在一定条件下分解的化学反应方程式
⑵已知0℃时X2Z的密度为a g/cm3,其晶胞中X2Z分子的空间排列方式与金刚石晶胞类似,相似的原因是 。两个X2Z分子间的最近距离为 pm(用a和NA表示)。 已知X2Y的升华热是51 kJ/mol,除氢键外,X2Z分子间还存在范德华力(11 kJ/mol),则X2Z晶体中氢键的“键能”是 kJ/mol。
⑶ WZ是一种功能材料,已被广泛用于电池电极、催化剂、半导体、玻璃染色剂等方面。工业上常以W(YZ3)2·6X2Z和尿素[CO(NH2)2]为原料制备。
①W2+的基态核外电子排布式为 ,其核外电子有 种运动状态。
②尿素分子中碳原子的杂化方式为 ,1 mol尿素分子中含有的σ键数为 。
③YZ3-的空间构型 。
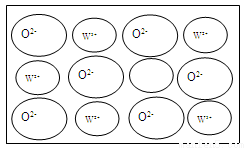
 ④WZ晶体的结构与NaCl相同,但天然的和绝大部分人工制备的晶体都存在各种缺陷,例如在某种WZ晶体中就存在如图所示的缺陷:一个W2+空缺,另有两个W2+被两个W3+所取代。其结果晶体仍呈电中性,但化合物中W和Z的比值却发生了变化。经测定某样品中W3+与W2+的离子数之比为6∶91。若该晶体的化学式为WxZ,则x= 。
④WZ晶体的结构与NaCl相同,但天然的和绝大部分人工制备的晶体都存在各种缺陷,例如在某种WZ晶体中就存在如图所示的缺陷:一个W2+空缺,另有两个W2+被两个W3+所取代。其结果晶体仍呈电中性,但化合物中W和Z的比值却发生了变化。经测定某样品中W3+与W2+的离子数之比为6∶91。若该晶体的化学式为WxZ,则x= 。
查看答案和解析>>
科目:高中化学 来源:2013-2014湖北省四校下学期期中考试高一化学试卷(解析版) 题型:选择题
已知:断开1molN≡N需要吸收akJ热量,断开1molH—H需要吸收bkJ热量,断开1molN—H需要吸收ckJ热量。向某密闭容器中通入1molN2和3molH2,在一定条件下发生反应:N2(g)+3H2(g)  2NH3(g)(放热反应)。下列描述中正确的是
2NH3(g)(放热反应)。下列描述中正确的是
A.N2和H2具有的总能量一定比NH3具有的总能量低
B.a、b、c三者的关系为:a+3b<2c
C.向密闭容器中通入1molN2和3molH2,反应放出的热量必为(6c―a―3b)kJ
D.形成1molN—H会放出ckJ热量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com