
| A£® | NaAČÜŅŗµÄpH£¾7£ØŹŅĪĀĻĀ£© | |
| B£® | pHŹŌÖ½ĻŌŹ¾0.1 mol/L HAČÜŅŗµÄpHĪŖ2”«3£ØŹŅĪĀĻĀ£© | |
| C£® | 0.1 mol/LµÄHClŗĶHAČÜŅŗ£¬Ē°Õߵĵ¼µēÄÜĮ¦Ć÷ĻŌøüĒæ | |
| D£® | HAČÜŅŗÄÜÓėCH3COONaČÜŅŗ·“Ӧɜ³ÉCH3COOH |
·ÖĪö ŅŖÖ¤Ć÷Ņ»ŌŖĖįHAĪŖČõĖį£¬æÉ“ÓÖ¤Ć÷HAŌŚČÜŅŗÖŠ“ęŌŚµēĄėĘ½ŗā”¢²»ÄÜĶźČ«µēĄė»ņ“Ó¶ŌÓ¦µÄĒæ¼īŃĪČÜŅŗ³Ź¼īŠŌµÄ½Ē¶Č·ÖĪö£¬ŅŌ“Ė½ā“šøĆĢā£®
½ā“š ½ā£ŗA£®NaAČÜŅŗµÄpH£¾7£ØŹŅĪĀĻĀ£©£¬ĖµĆ÷NaAĪŖĒæ¼īČõĖįŃĪ£¬Ė®½ā³Ź¼īŠŌ£¬æÉÖ¤Ć÷HAĪŖČõĖį£¬¹ŹA²»Ń”£»
B£®³£ĪĀĻĀ£¬²āµĆ0.01 mol/LHAČÜŅŗµÄpHĪŖ2”«3£¬ĖµĆ÷HAƻӊĶźČ«µēĄė£¬æÉÖ¤Ć÷HAĪŖČõĖį£¬¹ŹB²»Ń”£»
C£®HClĪŖĒæµē½āÖŹ£¬0.1 mol/LµÄHClŗĶHAČÜŅŗ£¬Ē°Õߵĵ¼µēÄÜĮ¦Ć÷ĻŌøüĒ棬ĖµĆ÷HAŌŚČÜŅŗÖŠ²æ·ÖµēĄė£¬ĪŖČõµē½āÖŹ£¬¹ŹC²»Ń”£»
D£®HAČÜŅŗÄÜÓėCH3COONaČÜŅŗ·“Ӧɜ³ÉCH3COOH£¬Ö»ÄÜÖ¤Ć÷ĖįŠŌHA±Č“×ĖįĒ棬¶ų“×ĖįĪŖČõĖį£¬ĪŽ·ØÖ¤Ć÷HAĪŖČõµē½āÖŹ£¬¹ŹDŃ”£»
¹ŹŃ”D£®
µćĘĄ ±¾Ģāæ¼²éĮĖČõµē½āÖŹµÄµēĄėĘ½ŗā¼°ĘäÓ¦ÓĆ£¬ĢāÄæÄѶČÖŠµČ£¬Ć÷Č·µēĄėĘ½ŗā¼°ĘäÓ°ĻģĪŖ½ā“š¹Ų¼ü£¬×¢ŅāÕĘĪÕĒæČõµē½āÖŹµÄøÅÄī¼°ÅŠ¶Ļ·½·Ø£¬ŹŌĢāÅąŃųĮĖѧɜµÄ·ÖĪö”¢Ąķ½āÄÜĮ¦¼°Įé»īÓ¦ÓĆÄÜĮ¦£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
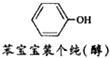
| A£® | ¼ī | B£® | Ģž | C£® | ĪŽ»śĪļ | D£® | ÓŠ»śĪļ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1molĘĻĢŃĢĒ×ī¶ąæÉŅŌÓė5mol½šŹōÄĘ·“Ó¦·Å³öĒāĘų | |
| B£® | 1molĘĻĢŃĢĒ×ī¶ąæÉŅŌÓė5molŅŅĖį·¢ÉśČ”“ś·“Ó¦ | |
| C£® | ÄÜ·¢ÉśŅų¾µ·“Ó¦ | |
| D£® | æÉÓėŠ”ĖÕ“ņČÜŅŗ·“Ӧư³öĘųÅŻ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Na+”¢HCO3-”¢SO42-”¢Br- | B£® | Mg2+”¢Na+”¢SO42-”¢Cl- | ||
| C£® | Na+”¢Cu2+”¢SO42-”¢NO3- | D£® | Na+”¢Ba2+”¢Cl-”¢SO42- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | C6H12O6 | B£® | £ØC6H10O5£©n | C£® | C12H22O11 | D£® | CF2Cl2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 0.1mol•L-1 Ļ”ĮņĖįÖŠŗ¬ÓŠSO42-Ąė×ÓøöŹżĪŖ0.1NA | |
| B£® | 0.1molNa2O2ÓėCO2ĶźČ«·“Ó¦£¬×ŖŅʵē×ÓŹżĪŖ0.2 NA | |
| C£® | ³£ĪĀ³£Ń¹ĻĀ£¬46 gµÄNO2ŗĶ46g µÄN2O4ŗ¬ÓŠµÄŌ×ÓŹżĻąµČ | |
| D£® | ±ź×¼×“æöĻĀ£¬22.4L SO3Ėłŗ¬µÄ·Ö×ÓŹżĪŖNA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
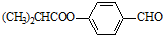 £®ŗĻ³ÉMµÄŅ»ÖÖĶ¾¾¶ČēĻĀ£ŗ
£®ŗĻ³ÉMµÄŅ»ÖÖĶ¾¾¶ČēĻĀ£ŗ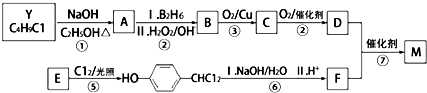
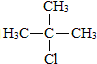 £®
£® £®
£®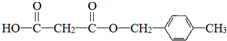 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| ŌÓÖŹ | ŹŌ¼Į | ·ÖĄė·½·Ø | ||
| A | ŅŅĶé | ŅŅĻ© | H2 | “ß»Æ×Ŗ»Æ |
| B | ŅŅĖįŅŅõ„ | ŅŅ“¼ | ±„ŗĶNa2CO3ČÜŅŗ | ·ÖŅŗ |
| C | äå±½ | äå | CCl4 | ŻĶČ” |
| D | ŅŅ“¼ | Ė® | ĪŽ | ÕōĮó |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | NaOH | B£® | Na2CO3 | C£® | NH4Cl | D£® | HCl |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com