
绿色化学要求利用化学反应原理从源头上消除污染。以铜为原料制备硫酸铜,下列四种原理设计,其中最能体现“绿色化学”要求的是
A.Cu +2H2SO4(浓)  CuSO4 +SO2↑+2H2O
CuSO4 +SO2↑+2H2O
B.Cu +Cl2  CuCl2 ,CuCl2+ H2SO4(浓)
CuCl2 ,CuCl2+ H2SO4(浓)  CuSO4 +2HCl↑
CuSO4 +2HCl↑
C.Cu + H2SO4 +H2O2  CuSO4 +2H2O
CuSO4 +2H2O
D. 3Cu +8HNO3=3Cu(NO3)2 +2NO↑+4H2O,Cu(NO3)2+H2SO4(浓)  CuSO4 +2HNO3↑
CuSO4 +2HNO3↑
 新思维寒假作业系列答案
新思维寒假作业系列答案科目:高中化学 来源:2013-2014江西省上饶市第二学期期末教学质量测试高二化学试卷(解析版) 题型:填空题
[化学———物质结构与性质]
已知X,Y,Z,Q为短周期非金属元素,R是长周期元素,X原子的电子占据2个电子层且原子中成对电子数是未成对电子数的2倍;Y的基态原子有7种不同运动状态的电子;Z元素在地壳中含量最多;Q是电负性最大的元素;R+离子只有三个电子层且完全充满电子?
回答下列问题:(答题时,X?Y?Z?Q?R用所对应的元素符号表示)
(1)X元素为 ,X?Y?Z中第一电离能最大的是 ?
(2)已知Y2Q2分子存在如图所示的两种结构(球棍模型,短线不一定代表单键):
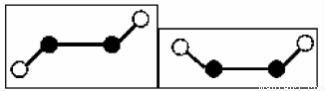
该分子中Y原子的杂化方式是 ?
(3)X与Y元素可以形成一种超硬新材料,其晶体部分结构如图所示,有关该晶体的说法
正确的是 (填正确答案编号)?

A.该晶体属于分子晶体 B.此晶体的硬度比金刚石还大
C.晶体的化学式是X3Y4 D.晶体熔化时破坏共价键
(4)有一种AB型分子与Y单质分子互为等电子体,它是一种常用的还原剂,其化学式为 ?
(5)R的基态原子的电子排布式为 ,R与Z形成的某离子晶体的晶胞结构如图,则该晶体的化学式为 ,该晶体的密度为a g·cm-3,则晶胞的体积是 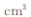 ?
?
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省盐城市高二下学期期终考试化学试卷(解析版) 题型:选择题
下列表示对应化学反应的离子方程式正确的是
A.碳酸钙溶于醋酸:CaCO3 + 2H+ = Ca2++ CO2↑+H2O
B.苯酚钠溶液中通入少量的CO2: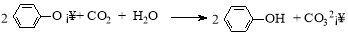
C.用铜做电极电解CuSO4溶液:2Cu2++2H2O 2Cu↓+O2↑+4H+
2Cu↓+O2↑+4H+
D.用银氨溶液检验乙醛中的醛基:CH3CHO+2Ag(NH3)2+ +2OH-
CH3COO-+NH4++3NH3+2Ag↓+H2O
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省盐城市高一下学期期末考试化学试卷(解析版) 题型:填空题
(12分)常见有机化合物转化关系如下图(部分反应条件已略去)。
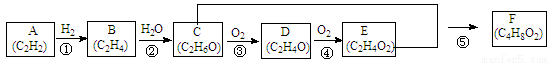
(1)A的结构式为 ;C中官能团的名称为 ;D物质的名称为 。
(2)属于取代反应的有 (填序号)。
(3)A光照生成G(分子式为C6H6),G分子中所有原子在同一平面,G既不能使酸性高锰酸钾溶液反应褪色,也不能使溴水反应褪色,则G的结构简式为 。
(4)H是E的同分异构体,能发生水解反应,H的结构简式可能为 。
(5)反应③的化学方程式为 ;反应⑤的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省盐城市高一下学期期末考试化学试卷(解析版) 题型:选择题
下列装置或操作能达到实验目的的是

A.蒸馏石油 B.除去甲烷中少量乙烯 C.验证化学能转变电能 D.制取乙酸乙酯
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省盐城市高一下学期期末考试化学试卷(解析版) 题型:选择题
只用一种试剂就可鉴别乙酸、葡萄糖溶液、淀粉溶液,这种试剂是
A.NaOH溶液B.稀H2SO4
C.Cu(OH)2悬浊液D.Na2CO3溶液
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省第二学期期中考试高二化学试卷(解析版) 题型:选择题
一定条件下,在体积为10 L的固定容器中发生反应:N2(g)+3H2(g)  ?2NH3(g) ΔH<0,反应过程如图:下列说法正确的是
?2NH3(g) ΔH<0,反应过程如图:下列说法正确的是

A.t1 min时正、逆反应速率相等。
B.X曲线表示NH3的物质的量随时间变化的关系
C.0~8 min,H2的平均反应速率v(H2)= mol·L-1·min-1
mol·L-1·min-1
D.10~12 min,升高温度使反应速率加快,平衡正向移动
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省淮安市高三第三次调研测试化学试卷(解析版) 题型:填空题
A、B、C、D为原子序数依次增大的前四周期元素,元素A原子最外层电子数比内层多3个,元素B基态原子核外有2个未成对电子,元素C的最高价和最低价代数和等于0,元素D位于周期表ⅥB族。
⑴判断离子AB2-离子的空间构型为 。
⑵元素A、C形成的化合物熔点很高,但比B、C形成的化合物熔点低,其原因是 。
⑶在A的氢化物(A2H4)分子中,A原子轨道的杂化类型是 。
⑷元素B与D形成的一种化合物广泛应用于录音磁带上,其晶胞如图所示。

该化合物的化学式为 。
⑸向D的氯化物DCl3溶液中滴加氨水可形成配合物[D(NH3)3(H2O)Cl2]Cl。
①离子D3+的外围电子排布式为 。
②1 mol该配合物中含配位键的数目为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com