
【题目】不能用水浴加热的实验是( )
A.苯的硝化反应
B.银镜反应实验
C.乙酸乙酯水解
D.由乙醇制乙烯
【答案】D
【解析】解:A.苯和浓硝酸、浓硫酸在50℃~60℃发生硝化反应生成硝基苯和水,该反应为C6H6+HNO3 ![]() C6H5NO2+H2O,需要水浴,故A正确;B.制备银镜时,用酒精灯的外焰给试管底部加热时温度太高,应水浴加热,如葡萄糖发生银镜反应的方程式为:CH2OH(CHOH)4CHO+2[Ag(NH3)2]OH
C6H5NO2+H2O,需要水浴,故A正确;B.制备银镜时,用酒精灯的外焰给试管底部加热时温度太高,应水浴加热,如葡萄糖发生银镜反应的方程式为:CH2OH(CHOH)4CHO+2[Ag(NH3)2]OH ![]() CH2OH(CHOH)4COONH4+2Ag↓+3NH3+H2O,故B正确;
CH2OH(CHOH)4COONH4+2Ag↓+3NH3+H2O,故B正确;
C.乙酸乙酯是重要的化工原料,沸点约77℃,其水解反应方程式为CH3COOC2H5+H2O ![]() CH3COOH+C2H5OH,实验需把试管放入70℃的水浴中加热,故C正确;
CH3COOH+C2H5OH,实验需把试管放入70℃的水浴中加热,故C正确;
D.因乙醇能分子内脱水生成乙烯,所以可用乙醇制乙烯,实验室利用加热到170℃时乙醇和浓硫酸混合溶液制取乙烯,反应方程式为CH3CH2OH ![]() CH2=CH2↑+H2O,反应的温度为170℃,超过沸水的温度,不能用水浴,故D错误;
CH2=CH2↑+H2O,反应的温度为170℃,超过沸水的温度,不能用水浴,故D错误;
故选D.
因为水的沸点是100℃,用水浴加热,所以“水浴”加热温度不可能超过100℃,水浴加热的温度是使反应容器内试剂受热温度均匀,据此即可解答.


科目:高中化学 来源: 题型:
【题目】将一定质量的Mg-Al合金投入100mL一定物质的量浓度的某HCl溶液中,充分反应。向反应后的溶液中逐滴加入一定物质的量浓度的NaOH溶液,生成沉淀的质量与所加NaOH溶液的体积关系如下图。回答下列问题:
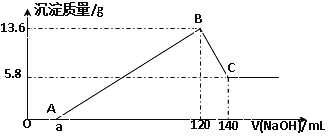
(1)写出OA段和BC段反应的离子方程式:
OA:________________________________ ; BC:_____________________________;
(2)原Mg-Al合金的质量是_____________。
(3)原HCl溶液的物质的量浓度是________________。
(4)所加NaOH溶液的物质的量浓度是____________。
(5)a的值是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,可逆反应A2(g)+B2(g)2C(g)达到平衡时,A2、B2和C的浓度分别为0.5mol/L、0.1mol/L、1.6mol/L,若用a、b、c分别表示A2、B2、C的初始浓度(mol/L),则:
(1)a、b应满足的关系是 .
(2)a的取值范围是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上可以利用反应Ca3(PO4)2+3H2SO4=3CaSO4+2H3PO4来制取磷酸,该反应属于
A.化合反应B.分解反应C.置换反应D.复分解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KClO3和浓盐酸在一定温度下反应,还原产物为黄绿色的易爆物二氧化氯。其变化可以表示为:![]() KClO3+
KClO3+![]() HCl(浓)―→
HCl(浓)―→![]() KCl+
KCl+![]() ClO2↑+
ClO2↑+![]() Cl2↑+
Cl2↑+![]() H2O
H2O
(1)请配平该化学方程式(未知系数填入框内)_____。
(2)浓盐酸在反应中显示出来的性质是________(填编号)。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3)5 ℃ 下将产物氯气0.1 mol溶于水配成1 L溶液,已知该溶液中氢氧根离子浓度最小,请将溶液中的其他成分按照其物质的量浓度从大到小顺序排列____________________(填分子或离子化学式,少写及顺序错误不得分)。
(4)若改变温度至70 ℃,发现KClO3和浓盐酸反应的氧化产物和还原产物均为二氧化氯气体,试写出反应的化学方程式:______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知酸性大小:羧酸>碳酸>酚.下列含溴化合物中的溴原子,在适当条件下都能被羟基(﹣OH)取代(均可称为水解反应),所得产物能跟NaHCO3溶液反应的是( )
A.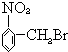
B.![]()
C.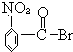
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮元素的氢化物和氧化物在工业生产和防建设中都有广泛的应用.请回答下列问题:
(1)氨气可由N2和H2反应制取,N2(g)+3H2(g)2NH3(g)反应过程的能量变化如图所示:已知1molN2分子中的化学键断裂时需要吸收942kJ的能量;1molH2分子中的化学键断裂时需要吸收436kJ的能量;形成1molN﹣H键时释放390.8kJ的能量. 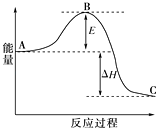
①图中E的大小对该反应热有无影响? . 该反应需要用铁触媒作催化剂,加铁触媒会使图中B点升高还是降低? , 理由 .
②图中△H=kJ/mol.
③如果反应速率v(H2)为0.15mol/(Lmin),则v(N2)=mol/(Lmin),v(NH3)= .
(2)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气. 已知:N2(g)+2O2(g)=N2O4(l)?△H=﹣19.5kJmol﹣1
N2H4(l)+O2(g)=N2(g)+2H2O(g)△H=﹣534.2kJmol﹣1
请写出肼和 N2O4反应的热化学反应方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏伽德罗常数,下列有关叙述错误的是( )
A.臭氧与氧气的混合气体4.8g中所含有的原子总数为0.3NA
B.标准状况下,2.24L单质气体中含有原子数为0.2NA
C.在常温常压下,3.4gNH3含有的电子数是2NA
D.含5.4 gAl3+的硫酸铝溶液中,含有的SO42﹣的数目是0.3NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com