
| A�� | Ũ����ͬ��Na2CO3��NaHCO3�����Һ�У�c��Na+����c��CO32-��=c��HCO3-����c��OH-����c��H+�� | |
| B�� | 0.1mol/L�ٴ�����Ȼ�梨�������Һ�У�ˮ���������������Ũ�ȴ�С˳���Ǣڣ��٣��� | |
| C�� | 0.1mol/L��NaHCO3��Һ�� C��Na+��+c��H+��=c��OH-��+c��HCO3-�� | |
| D�� | pH��ͬ�Ģ�CH3COONa��NaHCO3��NaClO������Һ��c��Na+�����ۣ��ڣ��� |
���� A��̼������ӵ�ˮ��̶ȴ���̼��������ӣ���c��HCO3-����c��CO32-����
B������Һ������ˮ�ĵ��룬�ܹ�ˮ�������Һ�ٽ���ˮ�ĵ��룻
C������̼��������Һ�еĵ���غ��жϣ�
D�������ζ�Ӧ�������Խǿ��������ӵ�ˮ��̶�Խ����pH��ͬʱ��ҺŨ��ԽС���ݴ˽��н��
��� �⣺A��Ũ����ͬ��Na2CO3��NaHCO3�����Һ�У�̼������ӵ�ˮ��̶ȴ���̼��������ӣ���c��HCO3-����c��CO32-������ȷ������Ũ�ȴ�СΪ��c��Na+����c��HCO3-����c��CO32-����c��OH-����c��H+������A����
B��0.1mol/L�ٴ�����Ȼ�梨�������Һ�У��٢�Ϊ����Һ����Һ��������������ˮ�ĵ��룬���Т���������Ũ�ȴ��ڢ٣������ˮ�ĵ���̶���С����Ϊǿ�������Σ�笠�����ˮ��ٽ���ˮ�ĵ��룬����ˮ���������������Ũ�ȴ�С˳���ǣ��ڣ��٣��ۣ���B��ȷ��
C��0.1mol/L��NaHCO3��Һ�У����ݵ���غ��֪��c��Na+��+c��H+��=c��OH-��+c��HCO3-��+2c��CO32-������C����
D����CH3COONa��NaHCO3��NaClO������Һ�����ԣ�CH3COOH��H2CO3��HClO����ˮ��̶ȣ��ۣ��ڣ��٣�pH��ͬʱ����ҺŨ�ȴ�СΪ���٣��ڣ��ۣ���Һ�е�c��Na+����СΪ���٣��ڣ��ۣ���D����
��ѡB��
���� ���⿼��������Ũ�ȴ�С�Ƚϣ���Ŀ�Ѷ��еȣ���ȷ�ε�ˮ��ԭ������Ӱ��Ϊ���ؼ���ע�����յ���غ㡢�����غ�ĺ��弰Ӧ�÷���������������ѧ���ķ������������Ӧ��������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ɫ��������ͨ��������������ͭ�Լ����ǵĺϽ���Ӧ�÷dz��㷺�Ľ������� | |
| B�� | ����ʱ�����������Ͼƺ�ʳ�ɼ�����ζ��������ζ�����������仯 | |
| C�� | ����ɢ������ֱ����1nm-100nm֮�䣬����Ϊ���壻�ŵ�ʱ��ӳ���䵽��Ļ�ϵĹ������γ����ڶ����ЧӦ | |
| D�� | Na2CO3•10H2O�ڸ��������ʧˮ��ľ�ĸ����ƽ�̿�����ڻ�ѧ�仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 4 | B�� | 7 | C�� | 8 | D�� | 11 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2-������ | B�� | 2-�һ����� | ||
| C�� | 3-������ | D�� | 1��3��3-�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���Ͳ��Ͼ�����ά�����ά�������л��߷��ӻ����� | |
| B�� | 14C��������������ļ�����14C��12C��Ϊͬ�������� | |
| C�� | �������ֿ���ʳƷ�ı��ʼ� | |
| D�� | ��������������Դ����������β����������������߿������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ȼú���ŷŴ�����CO��CO2��SO2��PM2.5������ο������ȾҲ������ȼú������أ�SO2��CO��CO2Ҳ�ǶԻ���Ӱ��ϴ�����壬�����ǵĺ������ơ��������Ż��������滷������Ч;����
ȼú���ŷŴ�����CO��CO2��SO2��PM2.5������ο������ȾҲ������ȼú������أ�SO2��CO��CO2Ҳ�ǶԻ���Ӱ��ϴ�����壬�����ǵĺ������ơ��������Ż��������滷������Ч;����| ʵ���� | �¶ȡ� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 20�� | B�� | 29�� | C�� | 30�� | D�� | 48�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
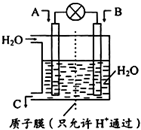
 �о���������ķ�Ӧ���������������Ի�������Ⱦ����Ҫ���壮�����¶Ⱦ�������Ļ�ѧ��Ӧ����������2NO��g��+O2��g��?2NO2��g��������ȴ�����¶ȵ����߶���С����������֪
�о���������ķ�Ӧ���������������Ի�������Ⱦ����Ҫ���壮�����¶Ⱦ�������Ļ�ѧ��Ӧ����������2NO��g��+O2��g��?2NO2��g��������ȴ�����¶ȵ����߶���С����������֪�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com